
”¾ĢāÄæ”æŹµŃéŹŅÖŠĄūÓĆCoCl2”¤6H2OĪŖŌĮĻÖĘȔȿĀČ»ÆĮł°±ŗĻīÜ[Co(NH3)6Cl3]µÄŹµŃé²½ÖčČēĻĀ£ŗ
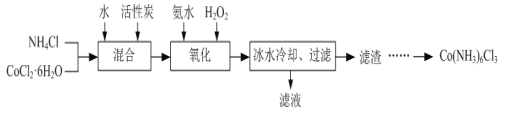
ŅŃÖŖ£ŗ¢ŁCo(NH3)6Cl3ŌŚ²»Ķ¬ĪĀ¶ČĻĀĖ®ÖŠµÄČܽā¶ČĒśĻßČēĶ¼”£
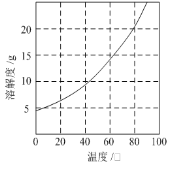
¢ŚŌŚCo(NH3)6Cl3ČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæŃĪĖįÓŠĄūÓŚ½į¾§”£
¢ŪKsp[Co(OH)2]=1.09”Į10-15£¬Ksp[Co(OH)3]=2”Į10-44”£
£Ø1£©ŌŚŹµŃé¹ż³ĢÖŠNH4Cl³ż×÷·“Ó¦ĪļĶā£¬»¹æÉ·ĄÖ¹ŌŚµĪ¼Ó°±Ė®Ź±c(OH-)¹ż“ó£¬ĘäŌĄķŹĒ______”£
£Ø2£©Ńõ»Æ¹ż³ĢÖŠ¼ÓČė°±Ė®ŗĶH2O2ŌŚČÜŅŗÖŠÉś³ÉCo(NH3)6Cl3”£
¢ŁŃõ»ÆŹ±ŠėĻČ¼ÓČė°±Ė®ŌŁ¼ÓČėH2O2£¬ĘäŌŅņŹĒ______”£
¢ŚøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______”£
¢Ū·“Ó¦Ź±ŠčŅŖæŲÖĘ·“Ó¦ĪĀ¶ČŌŚ50 ”ę~60 ”ęÖ®¼ä£¬æɲÉČ”µÄ¼ÓČČ·½Ź½ŹĒ______”£
£Ø3£©±łĖ®ĄäČ“µÄÄæµÄŹĒ______”£
£Ø4£©Ēė²¹³äĶźÕūÓɹżĀĖŗóĖłµĆĀĖŌü»ńČ”Co(NH3)6Cl3µÄŹµŃé·½°ø£ŗ½«ĀĖŌü¼ÓČė·ŠĖ®ÖŠ£¬³ä·Ö½Į°č£¬______£¬µĶĪĀøÉŌļ”££ØŹµŃéÖŠŠėŹ¹ÓƵďŌ¼Į£ŗŃĪĖį”¢ŅŅ“¼£©
”¾“š°ø”æNH4ClČÜÓŚĖ®µēĄė³öNH4+»įŅÖÖĘNH3”¤H2OµÄµēĄė·ĄÖ¹Co(OH)3µÄÉś³ÉH2O2+ 2CoCl2+2NH4Cl+10NH3”¤H2O£½2Co(NH3)6Cl3+ 12H2O»ņH2O2+ 2CoCl2+2NH4Cl+10NH3£½2Co(NH3)6Cl3+ 2H2OĖ®Ō”¼ÓČČ½µµĶČżĀČ»ÆĮł°±ŗĻīܵÄČܽā¶Č£¬Ģįøß²śĮæ³ĆČČ¹żĀĖ£¬ĻņĀĖŅŗÖŠ¼ÓČėÉŁĮæŃĪĖį£¬ÓƱłĖ®Ō”ĄäČ“ŗó¹żĀĖ£¬ŌŁÓĆÉŁŠķŅŅ“¼Ļ“µÓ
”¾½āĪö”æ
£Ø1£©ŌŚ¼īŠŌĢõ¼žĻĀČŻŅ×Éś³ÉĒāŃõ»ÆīܳĮµķ£¬Ņņ“ĖŌĮĻNH4ClµÄÖ÷ŅŖ×÷ÓĆ³żĮĖĢį¹©NH3ŅŌĶā£¬NH4ClČÜÓŚĖ®µēĄė³öNH4+»įŅÖÖĘNH3H2OµÄµēĄė£¬½µµĶČÜŅŗµÄ¼īŠŌ£¬¹Ź“š°øĪŖ£ŗNH4ClČÜÓŚĖ®µēĄė³öNH4+»įŅÖÖĘNH3H2OµÄµēĄė£»£Ø2£©¢ŁŃõ»ÆŹ±ŠėĻČ¼ÓČė°±Ė®ŌŁ¼ÓČėH2O2£¬ČōĻČ¼Ó¹żŃõ»ÆĒā£¬½«+2¼ÓīÜŃõ»Æµ½+3¼Ū£¬ŌŁ¼ÓČė°±Ė®£¬»įÓŠCo(OH)3µÄÉś³É£¬²»ĄūÓŚ²śĪļµÄÉś³É£»¹Ź“š°øĪŖ£ŗ·ĄÖ¹Co(OH)3µÄÉś³É£»¢ŚŃõ»Æ¹ż³ĢÖŠ¼ÓČė°±Ė®ŗĶH2O2ŌŚČÜŅŗÖŠÉś³ÉCo(NH3)6Cl3µÄ·“Ó¦ĪļĪŖ£ŗH2O2+2CoCl2+2NH4Cl+10NH3H2O=2Co(NH3)6Cl3+12H2O»ņH2O2+2CoCl2+2NH4Cl+10NH3=2Co£ØNH3£©6Cl3+2H2O£»¢ŪÓĆĖ®Ō”¼ÓČČæŲÖĘ·“Ó¦ĪĀ¶ČŌŚ50”ꔫ60”ęÖ®¼ä£»¹Ź“š°øĪŖ£ŗĖ®Ō”¼ÓČČ£»£Ø3£©ÓÉĶ¼2æÉÖŖCo£ØNH3£©6Cl3Ė®ÖŠµÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ųŌö“ó£¬ŌņĪŖĮĖ½µµĶČżĀČ»ÆĮł°±ŗĻīܵÄČܽā¶Č£¬Ģįøß²śĮ棬Ӧ±łĖ®ĄäČ“£»¹Ź“š°øĪŖ£ŗ½µµĶČżĀČ»ÆĮł°±ŗĻīܵÄČܽā¶Č£¬Ģįøß²śĮ棻£Ø4£©ÓɹżĀĖŗóĖłµĆĀĖŌü»ńČ”Co£ØNH3£©6Cl3µÄŹµŃé·½°ø£ŗ½«ĀĖŌü¼ÓČė·ŠĖ®ÖŠ£¬³ä·Ö½Į°č£¬³ĆČČ¹żĀĖ£¬ĻņĀĖŅŗÖŠ¼ÓČėÉŁĮæÅØŃĪĖį£¬ÓƱłĖ®Ō”ĄäČ“ŗó¹żĀĖ£¬ŌŁÓĆÉŁŠķŅŅ“¼Ļ“µÓ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµ±¹āŹųĶعżĻĀĮŠ·ÖÉ¢ĻµŹ±£¬ÄܹŪ²ģµ½¶”“ļ¶ūŠ§Ó¦µÄŹĒ£Ø £©
A.ŃĪĖįB.Fe(OH)3½ŗĢåC.ÕįĢĒČÜŅŗD.Na2SO4ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗpKa=-lgKa£¬25”ꏱ£¬H2SO3µÄ pKa1=1£®85£¬pKa2=7£®19£®ÓĆ0£®1molL-1NaOHČÜŅŗµĪ¶Ø20mL0£®1molL-1H2SO3ČÜŅŗµÄµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾(ĒśĻßÉĻµÄŹż×ÖĪŖpH)£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ( )
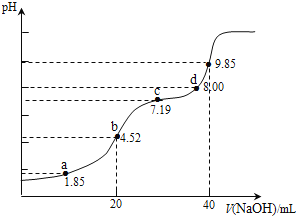
A£®aµćĖłµĆČÜŅŗÖŠ£ŗ2c(H2SO3)+c(SO32-)£¼0£®1 molL-1
B£®bµćĖłµĆČÜŅŗÖŠ£ŗc(H2SO3)+c(H+)=c(SO32-)+c(OH-)
C£®cµćĖłµĆČÜŅŗÖŠ£ŗc(Na+)£¼3c(HSO3 )
D£®dµćĖłµĆČÜŅŗÖŠ£ŗc(Na+)£¾c(SO32-)£¾c(HSO3-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ²»ŹōÓŚ“óĮæŌŖĖŲµÄŹĒ£Ø £©
A.Ć¾ŌŖĖŲB.¼ŲŌŖĖŲC.ĢśŌŖĖŲD.Į×ŌŖĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗŗ¬ÓŠ¢ŁNO3-¢ŚHCO3-¢ŪSO32-¢ÜCO32-¢ŻSO42-µČĪåÖÖŅõĄė×Ó”£ĻņĘäÖŠ¼ÓČėÉŁĮæµÄNa2O2¹ĢĢåŗó£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č»ł±¾±£³Ö²»±äµÄŹĒ(ÉčČÜŅŗĢå»żĪŽ±ä»Æ) ( ).
A.¢ŁB.¢Ł¢Ü¢ŻC.¢Ł¢Ū¢ŻD.¢Ł¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ”×éÉč¼Ę²»Ķ¬ŹµŃé·½°ø±Č½ĻCu2+”¢Ag+ µÄŃõ»ÆŠŌ”£
£Ø1£©·½°ø1£ŗĶعżÖĆ»»·“Ó¦±Č½Ļ
ĻņĖį»ÆµÄAgNO3ČÜŅŗ²åČėĶĖ棬Īö³öŗŚÉ«¹ĢĢ壬ČÜŅŗ±äĄ¶”£·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ_______£¬ĖµĆ÷Ńõ»ÆŠŌAg+£¾Cu2+”£
£Ø2£©·½°ø2£ŗĶعżCu2+”¢Ag+ ·Ö±šÓėĶ¬Ņ»ĪļÖŹ·“Ó¦½ųŠŠ±Č½Ļ
ŹµŃé | ŹŌ¼Į | ±ąŗż°ĻÖĻó | |
ŹŌ¹Ü | µĪ¹Ü | ||
| 1.0 mol/L KIČÜŅŗ | 1.0 mol/L AgNO3ČÜŅŗ | ¢ń£®²śÉś»ĘÉ«³Įµķ£¬ČÜŅŗĪŽÉ« |
1.0 mol/L CuSO4ČÜŅŗ | ¢ņ£®²śÉś°×É«³ĮµķA£¬ČÜŅŗ±ä»Ę | ||
¢Ł ¾¼ģŃ飬¢ńÖŠČÜŅŗ²»ŗ¬I2£¬»ĘÉ«³ĮµķŹĒ________”£
¢Ś ¾¼ģŃ飬¢ņÖŠČÜŅŗŗ¬I2”£ĶĘ²āCu2+×öŃõ»Æ¼Į£¬°×É«³ĮµķAŹĒCuI”£Č·ČĻAµÄŹµŃéČēĻĀ£ŗ
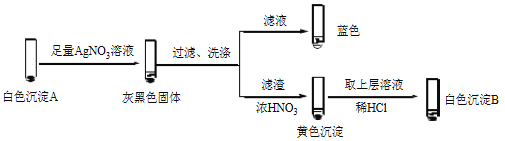
a£®¼ģŃéĀĖŅŗĪŽI2”£ČÜŅŗ³ŹĄ¶É«ĖµĆ÷ČÜŅŗŗ¬ÓŠ________£ØĢīĄė×Ó·ūŗÅ£©”£
b£®°×É«³ĮµķBŹĒ________”£
c£®°×É«³ĮµķAÓėAgNO3ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____£¬ĖµĆ÷Ńõ»ÆŠŌAg+£¾Cu2+”£
£Ø3£©·ÖĪö·½°ø2ÖŠAg+ Ī“ÄÜŃõ»ÆI- £¬µ«Cu2+Ńõ»ÆĮĖI-µÄŌŅņ£¬Éč¼ĘŹµŃéČēĻĀ£ŗ
±ąŗÅ | ŹµŃé1 | ŹµŃé2 | ŹµŃé3 |
ŹµŃé |
|
|
|
ĻÖĻó | ĪŽĆ÷ĻŌ±ä»Æ | aÖŠČÜŅŗ½Ļæģ±ä×Ų»ĘÉ«,bÖŠµē¼« ÉĻĪö³öŅų£»µēĮ÷¼ĘÖøÕėĘ«×Ŗ | cÖŠČÜŅŗ½ĻĀż±äĒ³»ĘÉ«£» µēĮ÷¼ĘÖøÕėĘ«×Ŗ |
£Øµē¼«¾łĪŖŹÆÄ«£¬ČÜŅŗÅØ¶Č¾łĪŖ 1 mol/L£¬b”¢dÖŠČÜŅŗpH”Ö4£©
¢Ł aÖŠČÜŅŗ³Ź×Ų»ĘÉ«µÄŌŅņŹĒ_______£ØÓƵē¼«·“Ó¦Ź½±ķŹ¾£©”£
¢Ś ”°ŹµŃé3”±²»ÄÜĖµĆ÷Cu2+Ńõ»ÆĮĖI-”£ŅĄ¾ŻŹĒæÕĘųÖŠµÄŃõĘųŅ²ÓŠŃõ»Æ×÷ÓĆ£¬Éč¼ĘŹµŃéÖ¤ŹµĮĖøĆŅĄ¾Ż£¬ŹµŃé·½°ø¼°ĻÖĻóŹĒ_______”£
¢Ū ·½°ø2ÖŠ£¬Cu2+ÄÜŃõ»ÆI-,¶ųAg+Ī“ÄÜŃõ»ÆI-µÄŌŅņ£ŗ_______”£
£Ø׏ĮĻ£ŗAg+ + I- = AgI”ż K1 =1.2”Į1016£»2Ag+ + 2I- = 2Ag”ż+ I2 K2 = 8.7”Į108£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æN2OĖ×³Ę”°Š¦Ęų”±£¬ŌųÓĆ×÷æÉĪüČėŠŌĀé×ķ¼Į”£ŅŌĻĀ·“Ó¦ÄܲśÉśN2O£ŗ3CO£«2NO2![]() 3CO2£«N2O”£ĻĀĮŠ¹ŲÓŚN2OµÄĖµ·ØÕżČ·µÄŹĒ(””””)
3CO2£«N2O”£ĻĀĮŠ¹ŲÓŚN2OµÄĖµ·ØÕżČ·µÄŹĒ(””””)
A. ÉĻŹö·“Ó¦ÖŠĆæÉś³É1 mol N2O£¬×ŖŅʵĵē×ÓŹżĪŖ3NA
B. µČĪļÖŹµÄĮæµÄN2OŗĶCO2ŗ¬ÓŠĻąµČµÄµē×ÓŹż
C. N2OÖ»¾ßÓŠŃõ»ÆŠŌ£¬ĪŽ»¹ŌŠŌ
D. N2O»įŃøĖŁÓėČĖĢåŃŖŗģµ°°×½įŗĻ£¬Ź¹ČĖÖŠ¶¾
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§Éč¼ĘČēĻĀĪ¢ŠĶŹµŃé×°ÖĆÓĆŅŌŃéÖ¤SO2µÄŠŌÖŹ£¬Ķعż·ÖĪöŹµŃ飬ĻĀĮŠ½įĀŪ±ķ“ļ²»ÕżČ·µÄŹĒ£Ø £©

A. aĆŽĒņĶŹÉ«£¬ŃéÖ¤SO2¾ßÓŠĘư׊Ō
B. bĆŽĒņĶŹÉ«£¬ŃéÖ¤SO2¾ßÓŠĖįŠŌŃõ»ÆĪļµÄŠŌÖŹ
C. cĆŽĒņĄ¶É«ĶŹČ„£¬ŃéÖ¤SO2¾ßÓŠ»¹ŌŠŌ
D. Ö»ÄÜÓĆÉÕ¼īČÜŅŗĪüŹÕĪ²Ęų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻÓĆŗ¬ĆĢ·ĻĮĻ(Ö÷ŅŖ³É·ÖMnO2£¬ŗ¬ÓŠÉŁĮæFe2O3”¢Al2O3”¢CuO”¢CaOµČ)ÓėŃĢĘųĶŃĮņ½ųŠŠĮŖŗĻ“¦Ąķ²¢ÖʱøMnSO4µÄĮ÷³ĢČēĻĀ£ŗ
ŅŃÖŖ£ŗ25”ꏱ£¬²æ·ÖĒāŃõ»ÆĪļµÄČܶȻż³£Źż(Ksp)ČēĻĀ±ķĖłŹ¾”£
ĒāŃõ»ÆĪļ | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
Ksp | 1.3”Į10-33 | 4.0”Į10-38 | 2.2”Į10-20 | 1.9”Į10-14 |
Ēė»Ų“š£ŗ
£Ø1£©³Įµķ1µÄ»ÆѧŹ½ĪŖ__________________”£
£Ø2£©ŹŅĪĀĻĀ£¬µ÷½ŚpHĪŖ5”£ŹŌĶعż¼ĘĖćĖµĆ÷“ĖŹ±Al3+”¢Fe3+ŅŃ³ĮµķĶźČ«£¬ĄķÓÉŹĒ_________”£ ”°¾»»Æ”±Ź±£¬¼ÓČė(NH4)2SµÄ×÷ÓĆĪŖ___________________”£
£Ø3£©”°Ėį»Æ”¢»¹Ō”±ÖŠ£¬·¢ÉśµÄĖłÓŠŃõ»Æ»¹Ō·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ__________________”£
£Ø4£©ŅŃÖŖ£ŗĀĖŅŗ3ÖŠ³żMnSO4Ķā£¬»¹ŗ¬ÓŠÉŁĮæ(NH4)2SO4”£(NH4)2SO4”¢MnSO4µÄČܽā¶ČĒśĻßČēĻĀĶ¼ĖłŹ¾”£¾Ż“ĖÅŠ¶Ļ£¬²Ł×÷”°I”±Ó¦ĪŖÕō·¢ÅØĖõ”¢____________”¢Ļ“µÓ”¢øÉŌļ”£

£Ø5£©¹¤ŅµÉĻæÉÓƵē½āĖįŠŌMnSO4ČÜŅŗµÄ·½·ØÖʱøMnO2£¬ĘäŃō¼«·“Ó¦Ź½ĪŖ________________”£
£Ø6£©25.35 g MnSO4”¤H2OѳʷŹÜČČ·Ö½ā¹ż³ĢµÄČČÖŲĒśĻß(ѳʷ֏ĮæĖęĪĀ¶Č±ä»ÆµÄĒśĻß)ČēĻĀĶ¼ĖłŹ¾”£1150”ꏱ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________________”£
 ӣ
ӣ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com