
 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质: ②
② ③
③ ④
④ ,
,| A、取代、消去、酯化、加成 |
| B、酯化、消去、氧化、取代 |
| C、酯化、取代、氧化、取代 |
| D、消去、消去、氧化、取代 |
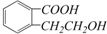 中含-COOH和-OH,发生分子内酯化反应生成①,发生-OH的消去反应生成②,发生氧化反应生成③,发生-OH的取代反应生成④,以此来解答.
中含-COOH和-OH,发生分子内酯化反应生成①,发生-OH的消去反应生成②,发生氧化反应生成③,发生-OH的取代反应生成④,以此来解答.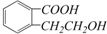 中含-COOH和-OH,发生分子内酯化反应生成①,该反应属于酯化反应,也属于取代反应;
中含-COOH和-OH,发生分子内酯化反应生成①,该反应属于酯化反应,也属于取代反应;

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、豆科植物的固氮菌将空气中的氮变成氨吸收 |
| B、闪电能将氮转化为氮的氧化物随雨水成硝酸被植物根系吸收 |
| C、工业上在一定条件下用氮气和氢气直接转化为氨 |
| D、在一定条件下,将氨直接氧化成一氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素处于最高价态时一定有强氧化性;同理元素处于最低价态时一定具有强还原性 |
| B、将FeCl2溶液与稀HNO3混合离子反应方程式:Fe2++4H++NO3-═Fe3++NO↑+2H2O |
| C、HF、Al(OH)3、氨水都是弱电解质 |
| D、蛋白质与硝酸的颜色反应、酸碱指示剂的变色反应均属化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Z的最高价氧化物对应的水化物为强酸 |
| D、XW2分子中各原子最外层电子均达到8电子结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com