
| A. | 9.6g | B. | 9.8g | C. | 19.2g | D. | 无法确定 |
分析 加入NaOH溶液至三种金属阳离子刚好全部转化为沉淀,反应后溶质为硫酸钠,根据n=$\frac{m}{M}$计算出氢氧化钠的物质的量,从而得出硫酸根离子的物质的量,再根据m=nM计算出磷酸根离子子的质量.
解答 解:8g氢氧化钠的物质的量为:n(NaOH)=$\frac{8g}{40g/mol}$=0.2mol,
溶液中含Mg2+,Al3+,Fe3+,SO42-四种离子,加入NaOH溶液至三种金属阳离子刚好全部转化为沉淀,此时溶质为硫酸钠,根据钠离子守恒可知硫酸钠的物质的量为:n(Na2SO4)=n(SO42-)=$\frac{1}{2}$n(NaOH)=0.2mol×$\frac{1}{2}$=0.1mol,
0.1mol硫酸根离子的质量为:96g/mol×0.1mol=9.6g,
故选A.
点评 本题考查了离子反应的计算,题目难度中等,明确发生反应实质及质量守恒定律为解答关键,注意掌握物质的量与摩尔质量之间的关系,试题侧重考查学生的分析、理解能力及化学计算能力.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
| 编号 | 实验目的 | 反应物 | 反应前 溶液的pH | 温度 |
| 1 | 对照组 | O3+NaI+H2SO4 | 5.2 | 25℃ |
| 2 | ①探究FeCl2对反应速率的影响 | O3+NaI+H2SO4+FeCl2 | 5.2 | ②25℃ |
| 3 | 探究温度对反应速率的影响 | O3+NaI+H2SO4 | ③5.2 | 5℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,该现象说明可用CCl4从碘水中萃取碘. | |
| B. | 向某水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明原溶液中一定含有SO42-离子 | |
| C. | 将饱和氯化铁溶液煮沸,可制得氢氧化铁胶体 | |
| D. | 稀释浓硫酸时将浓硫酸沿烧杯壁慢慢注入水中并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、Cu2+、Cl-、SO42- | D. | Na、H+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:4 | B. | 2:1:3 | C. | 3:4:2 | D. | 4:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g S8单质中含有的S-S键个数为6.02×1023 | |
| B. | 12.4g白磷中含有磷原子数为0.4NA | |
| C. | 常温常压下,1mol氦气含有的核外电子数为4NA | |
| D. | 0.1mol OH-含NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
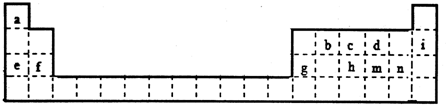
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯在空气中燃烧 | |
| B. | 乙烯在一定条件下跟HCl反应 | |
| C. | 苯与液溴在FeBr3催化下生成溴苯 | |
| D. | 苯在一定条件下跟H2反应生成环己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com