
| A. | 混合物中铝、铁的物质的量之比1:2 | |
| B. | 混合物与稀硝酸反应后的溶液还能溶解1.28g Cu | |
| C. | 将0.28mol气体通人水中并完全被吸收时,需要消耗0.14mol氧气 | |
| D. | 10.7g固体为Al(OH)3和Fe(OH)3的混合物 |
分析 铝、铁与稀硝酸反应生成的气体为NO,280mL 4mol•L-1的稀硝酸中含有硝酸的物质的量为:4mol/L×0.28L=1.12mol,500mL3mol•L-1的Na0H溶液中含有氢氧化钠的物质的量为:3mol/L×0.5L=1.5mol,当NaOH与铝离子、铁离子生成沉淀最大时,此时溶质为硝酸钠,根据N元素守恒消耗氢氧化钠的物质的量为:1.12mol-0.28mol=0.84mol,剩余NaOH的物质的量为:1.5mol-0.84mol=0.66mol,
当11g完全为Al时,生成氢氧化铝沉淀的物质的量为:$\frac{11g}{27g/mol}$≈0.41mol,根据质量守恒可知生成氢氧化铝沉淀的最大物质的量为0.41mol,所以剩余的0.66mol氢氧化钠溶液能够将所有氢氧化铝溶解,即:最终得到的10.7g固体不含Al(OH)3;
由于经过充分搅拌、过滤、洗涤、干燥后称量得到10.7g固体,则10.7g完全为氢氧化铁,10.7g氢氧化铁的物质的量为:$\frac{10.7g}{107g/mol}$=0.1mol,根据铁元素守恒可知原混合物中含有铁的质量为:56g/mol×0.1mol=5.6g,混合物中铝的物质的量为:$\frac{11g-5.6g}{27g/mol}$=0.2mol,据此进行解答.
解答 解:铝、铁与稀硝酸反应生成的气体为NO,280mL 4mol•L-1的稀硝酸中含有硝酸的物质的量为:4mol/L×0.28L=1.12mol,500mL3mol•L-1的Na0H溶液中含有氢氧化钠的物质的量为:3mol/L×0.5L=1.5mol,当NaOH与铝离子、铁离子生成沉淀最大时,此时溶质为硝酸钠,根据N元素守恒消耗氢氧化钠的物质的量为:1.12mol-0.28mol=0.84mol,剩余NaOH的物质的量为:1.5mol-0.84mol=0.66mol,
当11g完全为Al时,生成氢氧化铝沉淀的物质的量为:$\frac{11g}{27g/mol}$≈0.41mol,根据质量守恒可知生成氢氧化铝沉淀的最大物质的量为0.41mol,所以剩余的0.66mol氢氧化钠溶液能够将所有氢氧化铝溶解,即:最终得到的10.7g固体不含Al(OH)3;
由于经过充分搅拌、过滤、洗涤、干燥后称量得到10.7g固体,则10.7g完全为氢氧化铁,10.7g氢氧化铁的物质的量为:$\frac{10.7g}{107g/mol}$=0.1mol,根据铁元素守恒可知原混合物中含有铁的质量为:56g/mol×0.1mol=5.6g,混合物中铝的物质的量为:$\frac{11g-5.6g}{27g/mol}$=0.2mol,
A.混合物中铝、铁的物质的量之比=0.2mol:0.1mol=2:1,故A错误;
B.0.2mol铝、0.1mol铁完全反应转化成硝酸铝、硝酸铜消耗硝酸的物质的量为:(0.2mol+0.1mol)×4=1.2mol,而硝酸的物质的量为1.12mol,说明硝酸不足,反应生成的是硝酸铝、硝酸亚铁和硝酸铁;混合物与稀硝酸反应后生成的亚铁离子、铁离子的总物质的量为0.1mol,根据电子守恒,失去电子总物质的量为:0.28mol×3-0.2mol×3=0.24mol,设生成亚铁离子的物质的量为x,铁离子的物质的量为y,则x+y=0.1、2x+3y=0.24,解得:y=0.04mol、x=0.06mol,0.06mol铁离子与铜完全反应消耗铜的物质的量为:$\frac{0.04mol}{2}$=0.02mol,质量为:64g/mol×0.02mol=1.28g,故B正确;
C.0.28mol为NO,根据反应4NO+2H2O+3O2=4HNO3可知,0.28molNO完全反应消耗氧气的物质的量为:0.28mol×$\frac{3}{4}$=0.21mol,故C错误;
D.根据分析可知,得到的10.7g固体为氢氧化铁,不含氢氧化铝,故D错误;
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,正确判断得到的10.7g固体组成为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常温下,0.1molH2O2中含有极性共价键的数目为0.1NA | |
| B. | 电解饱和食盐水时,当阴极产生22.4LH2时,电路中转移的电子数为2NA | |
| C. | 100mL12mol•L-1的浓HNO3与过量Cu反应转移电子的数目为0.6NA | |
| D. | 标准状况下,11.2L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
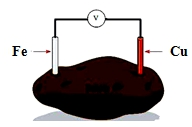
| A. | Fe用作正极 | B. | Cu片质量减少 | ||
| C. | 电子由Fe并经导线流向Cu片 | D. | 实现了电能向化学能的转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
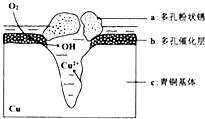 铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:
铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向容量瓶或分液漏斗中注入溶液时,应该将两者口部的玻璃塞倒置在桌面上 | |
| B. | 在实验室做蒸馏实验的装置中用到两个铁架台、三个单孔胶塞 | |
| C. | 将等体积不同浓度的酸性高锰酸钾分别滴入等浓度体积的草酸溶液中,依据褪色快慢,比较浓度对翻译速率的影响 | |
| D. | 过量的浓硫酸与铜屑共热,能得到澄清透明的蓝色溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
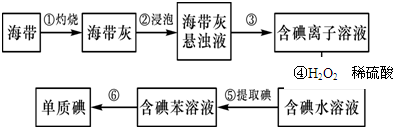
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 棉花和蚕丝的主要成分都是纤维素 | |
| B. | 蛋白质在一定条件发生水解反应生成葡萄糖 | |
| C. | 酶是一类具有催化作用的蛋白质,其催化作用有很强的专一性、高效性 | |
| D. | 食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com