
| A. | 质量为18g | B. | 含有NA个氧原子 | ||
| C. | 标准状况下体积约为22.4L | D. | 含有NA个水分子 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 定容时,仰视刻度线 | B. | 称量用了生锈的砝码 | ||
| C. | 未洗涤溶解NaOH的烧杯 | D. | 容量瓶未经过干燥即用来配制溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离碘单质和四氯化碳的混合物需要烧杯、玻璃棒和漏斗 | |
| B. | 用湿润的pH试纸测定溶液的pH一定会产生误差 | |
| C. | 实验室可以向浓硫酸中滴加浓盐酸制取少量氯化氢 | |
| D. | 用浓氨水可以除去试管内壁银镜 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
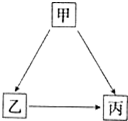 甲、乙、丙三种物质有如图所示的转化关系.
甲、乙、丙三种物质有如图所示的转化关系.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质参加和单质生成的化学反应一定是氧化还原反应 | |
| B. | 盐酸是强酸,所以盐酸是强电解质 | |
| C. | 向FeCl3饱和溶液滴加NaOH溶液可制备Fe(OH)3胶体 | |
| D. | 化合反应不一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | mg的CO和H2混合气体充分燃烧后,生成的气体通入Na2O2固体中,固体质量增重mg | |
| B. | 将一定量的CO2气体通入足量的Na2O2固体中,固体量增重2.8g,则反应中有0.1mol电子转移 | |
| C. | 相同质量的铝分别与足量的盐酸和NaOH溶液反应,生成气体物质的量之比为1:3 | |
| D. | NaAlO2溶液中逐滴滴入盐酸至过量,生成的沉淀随着加入的元素所发生的变化如图所示: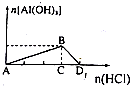 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
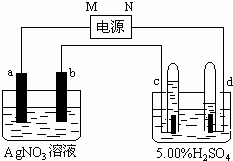 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.请回答下列问题.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com