
| A. | 该氯原子的相对原子质量为$\frac{a}{b}$ | |
| B. | m g该氯原子的物质的量为$\frac{m}{a{N}_{A}}$mol | |
| C. | 该氯原子的摩尔质量为aNAg | |
| D. | a g该氯原子所含的电子数为17 mol |
分析 A.某一原子的相对原子质量是指:以一个碳-12原子质量的$\frac{1}{12}$作为标准,该原子的质量跟一个碳-12原子质量的1/12的比值;
B.已知质量求物质的量,运用公式n=m/M求;
C.摩尔质量的单位为g/mol;
D.氯原子的质子数为17,1个氯原子所含的电子数是17.
解答 解:A.氯原子的相对原子质量为$\frac{12a}{b}$,故A错误;
B.根据公式n=$\frac{m}{M}$,一个该氯原子的质量是a,则1mol该氯原子的质量(摩尔质量)为(aNA)g/mol,那么mg该氯原子的物质的量即为$\frac{m}{a{N}_{A}}$mol,故B正确;
C.一个该氯原子的质量是a,1mol该氯原子的质量(摩尔质量)为(aNA)g/mol,单位错误,故C错误;
D.一个该氯原子的质量是a,a g该氯原子个数NA,1个氯原子所含的电子数是17个,该氯原子所含的电子数为17 NA,故D错误.
故选B.
点评 本题考查了物质的量的计算,题目涉及相对原子质量、物质的量、摩尔质量等概念,平时学习是需理解这些概念与相关概念的区别和联系,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
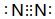 .
. NH3•H2O
NH3•H2O  NH4++OH-.
NH4++OH-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、CO32-、NO3- | B. | Mg2+、NH4+、SO42-、Cl- | ||
| C. | Fe3+、K+、NO3-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲烷与丙烷互为同系物 | |
| B. | 甲烷的一氯代物只有一种结构证明甲烷是正四面体结构而非平面正方形结构 | |
| C. | 甲烷、乙烷、丙烷中的化学键都是极性共价键 | |
| D. | 乙烷和氯气在光照的条件下可发生取代反应,生成多种氯代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学变化一定伴随着能量变化 | |
| B. | 升高温度或加入催化剂,可以改变化学反应的反应热 | |
| C. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| D. | 热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,3-二乙基-1-戊烯 | D. | 3,4-二甲基-4-乙基己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com