
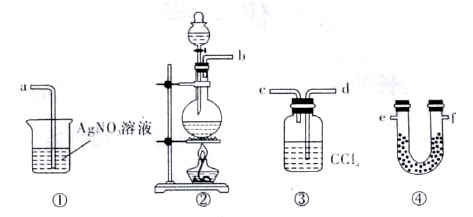
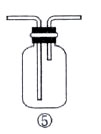
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
 ;
; 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
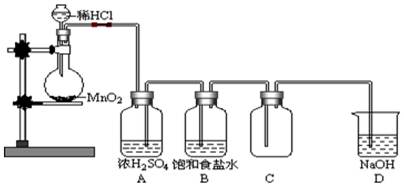
 述装置图中的错误(有几处答几处)
述装置图中的错误(有几处答几处)查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | — | 315 | — |
| 熔点/℃ | -70.0 | -107.2 | — | — | — |
| 升华温度/℃ | — | — | 180 | 300 | 162 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
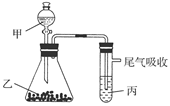
| | 甲 | 乙 | 丙 | 结论 |
| A | 水 | 电石 | 溴水 | 稳定性:水>C2H2>Br2 |
| B | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| C | 盐酸 | FeS | 溴水 | 还原性:S2->Br->Cl- |
| D | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4<Cl2<Br2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 为 ,实验中为了减缓反应速率,常用 代替水,若实验中产生的气体存在难闻的气味,可以用_________________(填试剂)加以除去。
为 ,实验中为了减缓反应速率,常用 代替水,若实验中产生的气体存在难闻的气味,可以用_________________(填试剂)加以除去。 化硫,他们设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:
化硫,他们设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:
 (填字母)
(填字母)| A.④②①③ | B.①②①③ | C.①②①④ | D.④②①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响? (填“偏高”、”偏低”或“无影响”);
制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响? (填“偏高”、”偏低”或“无影响”);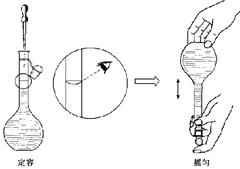
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
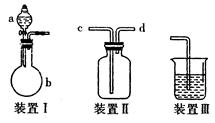
| 装置序号 | 仪器中所加物质名称 | 现象 |
| | | |
| | | |
| | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com