
【题目】下列属于碱的是( )
A. MgOB. Ca(OH)2C. H2OD. Na2CO3
科目:高中化学 来源: 题型:
【题目】电解尿素[CO(NH2)2]是一种能耗很低的制氢方法,其工作原理如图所示,总反应为CO(NH2)2+2OH-![]() N2↑+3H2↑+CO32-。下列说法错误的是
N2↑+3H2↑+CO32-。下列说法错误的是

A. 阴极的材料可选择钢铁制品
B. 电解池工作时,阳极区域溶液的pH减小
C. 阳极的电极反应式为CO(NH2)2+8OH--6e-==N2↑+ CO32-+6H2O。
D. 若电路中通过3 mol 电子,则生成气体的总体积为33. 6L(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素的原子序数依次增大,A原子无中子,B的单质在空气中含量最多,C、D元素同主族且原子序数D为C的二倍,E元素的价电子排布式为(n-l)dn+6ns1。回答下列问题:
(1)元素B在周期表中的位置是 ;E元素的元素符号为 ,它能形成E+的原因为 。
(2)D元素基态原子的核外电子轨道排布图为![]() 。
。
(3)A元素与C元素形成两种常见的化合物,其原子个数比分别为2:1和1:1,两种化合物可以任意比互溶,原因是 ;其中一种化合物可在酸性条件下将KMnO4还原为Mn2+,相关反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀产生的工业废水含有的重金属离子(Cu2+、Ni2+等)和CN形成难以除去的络合物,用电解法制备高铁酸钠(Na2FeO4)处理废水是目前比较先进的方法。已知氰化氢有毒易挥发。电解装置如图所示,下列选项正确的是( )
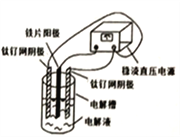
A. 铁片连接电源的负极
B. 电解时,每生成lmolFeO42-,转移电子3mol
C. CN被氧化成CO2和N2,Cu2+、Ni2+形成难溶碱而除去
D. 已知HFeO4-的氧化性比FeO42-更强,故pH<7时处理废水效率更高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物X分子中碳氢质量比为6:1,E的结构简式为(![]() ),请根据下列转化关系图回答问题:
),请根据下列转化关系图回答问题:
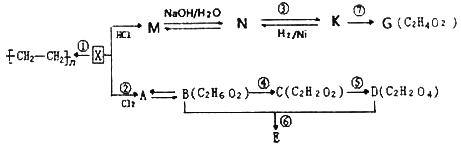
(1)K中官能团的结构式为:__________,C的化学名称是____________。
(2)写出下列反应的反应类型:M→N____________,反应⑤____________________。
(3)写出物质A的结构简式:______________________________________________。
(4)若物质K与银氨溶液反应,化学方程式为__________________________________。
(5)用一种世纪可鉴别N、K、G三种物质,该化学试剂为__________________________。
(6)写出下列反应的化学方程式:
反应⑥_________________________。
(7)与G互为同系物,且比G多3个碳原子的物质的同分异构体个数共有_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2NO2![]() N2O4的可逆反应中,下列状态一定属于平衡状态的是( )
N2O4的可逆反应中,下列状态一定属于平衡状态的是( )
A. N2O4和NO2的分子数比为1:2
B. N2O4和NO2的浓度相等
C. 体系的颜色不再改变
D. 单位时间内有1molN2O4转化为NO2的同时,有2molNO2转化为N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图甲是一种利用微生物将废水中的尿素(H2NCONH2,氮元素显-3价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )
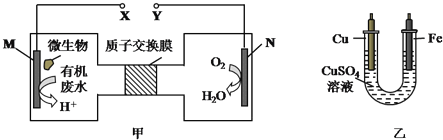
A.H+透过质子交换膜由左向右移动
B.铜电极应与Y相连接
C.M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+
D.当N电极消耗0.25mol气体时,则铁电极增重16g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com