
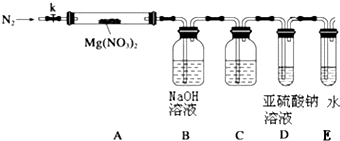
 某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.分析 (1)NO2在碱性条件下自身发生氧化还原反应,与氢氧化钠反应生成NaNO3和NaNO2;
(2)根据氧化还原反应化合价升降相等判断;
(3)为检验是否生成氧气,应将装置内的氧气排尽;加热Mg(NO3)2固体,固体质量减小,如生成红棕色气体,则有NO2生成;
(4)亚硫酸钠具有还原性,可被氧气氧化,也可被二氧化氮氧化;
(5)亚硫酸钠溶液与氧气反应没有明显现象,结合亚硫酸钠溶液呈碱性,硫酸钠溶液呈中性判断;
(6)如果分解产物中有O2存在,但没有检测到,可能原因是二氧化氮、氧气与水反应.
解答 解:(1)NO2在碱性条件下自身发生氧化还原反应,与氢氧化钠反应生成NaNO3和NaNO2,反应的方程式为2NO2+2NaOH=NaNO3+NaNO2+H2O,
故答案为:2NO2+2NaOH=NaNO3+NaNO2+H2O;
(2)由于丙产物中化合价只有降低情况,没有升高,不满足氧化还原反应的特征,故答案为:不符合氧化还原反应原理;
(3)为检验是否生成氧气,应将装置内的氧气排尽,避免对产物O2的检验产生干扰,加热Mg(NO3)2固体,固体质量减小,如生成红棕色气体,则有NO2生成,
故答案为:避免对产物O2的检验产生干扰(或其它合理答案);固体减少;产生红棕色气体,溶液中有气泡冒出;
(4)亚硫酸钠具有还原性,可被氧气氧化,也可被二氧化氮氧化,通入之前,还需在BD装置间增加滴有酚酞的氢氧化钠溶液,可确保二氧化氮已被除尽,防止干扰氧气的检验,
故答案为:确保二氧化氮已被除尽,防止干扰氧气的检验;
(5)亚硫酸钠溶液与氧气反应没有明显现象,结合亚硫酸钠溶液呈碱性,硫酸钠溶液呈中性判断,可滴加几滴酚酞试剂,如溶液由红色变为无色,说明有氧气生成,
故答案为:亚硫酸钠溶液与氧气反应没有明显现象,难以判断反应是否发生了;几滴酚酞试剂;
(6)如果分解产物中有O2存在,但没有检测到,可能原因是二氧化氮、氧气与水反应,发生方程式为4NO2+O2+2H2O=4HNO3 或4NO2+O2+4NaOH=4NaNO3+2H2O,
故答案为:4NO2+O2+2H2O=4HNO3 或4NO2+O2+4NaOH=4NaNO3+2H2O.
点评 本题为实验探究题目,侧重于学生的分析、实验能力的考查,为高考常见题型,答题时主要在把握物质的性质基础上把握实验的原理、目的以及相关实验的基本操作,题目难度不大,但需夯实基础.


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:解答题
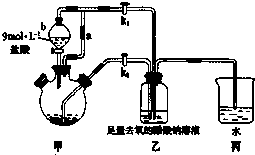 醋酸亚铬水合物[Cr(CH3COO)2]2•2H2O(相对分子质量为376)是一种为红棕色晶体,极易被氧气氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂).
醋酸亚铬水合物[Cr(CH3COO)2]2•2H2O(相对分子质量为376)是一种为红棕色晶体,极易被氧气氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制一定物质的量浓度的硫酸溶液时,定容时俯视会造成溶液浓度偏高 | |
| B. | 量取15.20mL AgNO3溶液可以用酸式滴定管 | |
| C. | 过滤完毕,洗涤沉淀时应该向漏斗中加水至没过沉淀,用玻璃棒搅拌充分洗剂,重复2~3次 | |
| D. | 蒸发浓缩CuSO4溶液时,要用玻璃棒搅拌防止溶液溅出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 催化剂组成 | 1 | 2 | 3 |
| WO3 W α-Fe2O3 | 65% 5% 30% | 65% 10% 25% | a b 20% |
| 六价铬去除率 | 60.2% | 80% | 72.9% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
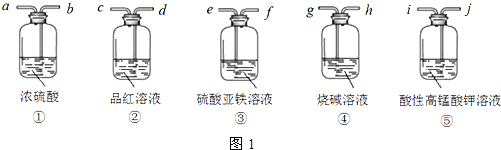
| 苯甲酸 | 乙醇 | 苯甲酸乙酯 | |
| 熔点/℃ | 122.4 | -114.1 | -34.6 |
| 沸点/℃ | 249 | 78.3 | 212.6 |
| 密度/g•cm-3 | 1.2659 | 0.816 | 1.05 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
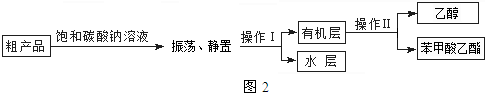
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸银、氨水 | B. | 硫酸亚铁溶液、氢氧化钠溶液 | ||
| C. | 明矾溶液、氢氧化钡溶液 | D. | 氯化铝溶液、氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
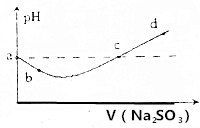
| A. | a点表示的溶液中存在3种分子,3种离子 | |
| B. | b点溶液中不存在SO2 | |
| C. | c点溶液中c(Na+)=2c(HSO3-)+2c(SO32-) | |
| D. | d点溶液中不存在HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消耗1 mol CH3CH2OH时转移电子的物质的量为4mol | |
| B. | 1mol/L CH3COOH溶液中含有σ键的数目为7NA个 | |
| C. | H2F+、NH2-、H2S、CH4均与H2O互为等电子体 | |
| D. | 在配合物[Cr(H2O)6]3+中,H、O原子与中心离子Cr3+形成配位键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com