
| A. | 3:2 | B. | 4:3 | C. | 1:1 | D. | 8:9 |
分析 铝热剂中只有Al和氢氧化钠反应,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,铝热剂发生反应2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,反应后的物质中只有Fe和稀盐酸反应生成氢气,根据铝热反应知,Al和Fe的物质的量之比为1:1,根据转移电子计算生成气体体积之比.
解答 解:铝热剂中只有Al和氢氧化钠反应,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,铝热剂发生反应2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,反应后的物质中只有Fe和稀盐酸反应生成氢气,根据铝热反应知,Al和Fe的物质的量之比为1:1,假设Al、Fe的物质的量都是2mol,2molAl在反应中转移6mol电子、2molFe在反应中转移4mol电子,所以2molAl和NaOH完全反应生成3mol氢气、2molFe和稀盐酸反应生成2mol氢气,根据V=nVm知,相同条件下生成氢气体积之比等于氢气的物质的量之比=3mol:2mol=3:2,故选A.
点评 本题考查混合物的计算,侧重考查学生分析计算能力,利用转移电子进行计算能化繁为简,提高解题效率,还可以根据方程式进行计算,题目难度不大.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醛与新制Cu(OH)2悬浊液反应生成红色的Cu2O沉淀 | |
| B. | 银镜反应中醛发生的是还原反应 | |
| C. | 甲醛、乙醛、丙醛都没有同分异构体 | |
| D. | 醛类催化加氢后都能得到饱和一元醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.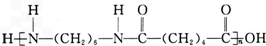 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HXO3 XO2 | B. | HXO2 X2O3 | C. | H3XO3 X2O3 | D. | H3XO4 X2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Fe3+、Cl-、NO3- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、SO42-、Na+ | D. | Na+、K+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成n mol A2的同时消耗n mol A2 | |
| B. | 容器内的各组分的浓度不随时间变化而变化 | |
| C. | 单位时间内生成2n mol AB的同时生成n mol B2 | |
| D. | A2、B2和AB的分子数之比为1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1=△H2 | B. | △H1>△H2 | C. | △H1<△H2 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com