
【题目】下表列出了①~⑨九种元素在周期表中的位置。
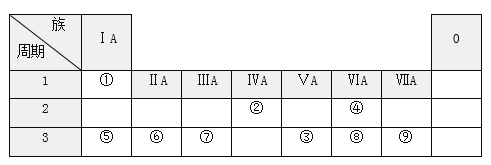
请按要求回答下列问题:
(1)元素⑦的原子结构示意图______________________。①、④按原子个数比为1:1组成的分子的电子式____________________;由②、④两种元素组成的一种化合物的结构式________________;
(2)⑤⑥两种元素的原子半径由大到小的顺序是____________(填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是________(填化学式)。
(4)元素③的气态氢化物和元素⑧的气态氢化物易于制备的是___________(填化学式)。
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为_________________________________________。
(6)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式__________________ ;一种离子化合物的化学式_________。
【答案】![]()
![]() O=C=O Na>Mg H2SO4 H2S Al(OH)3+OH-=AlO2-+2H2O H2O Na2O
O=C=O Na>Mg H2SO4 H2S Al(OH)3+OH-=AlO2-+2H2O H2O Na2O
【解析】
根据元素在周期表中的位置知①②③④⑤⑥⑦⑧⑨分别是H、C、P、O、Na、Mg、Al、S、Cl元素。
(1) 元素⑦为Al,原子结构示意图为:![]() ;①、④按原子个数比为1:1组成的分子为:H2O2,电子式为:
;①、④按原子个数比为1:1组成的分子为:H2O2,电子式为:![]() ;由②、④两种元素组成的化合物为:CO2, 结构式为:O=C=O。答案为:
;由②、④两种元素组成的化合物为:CO2, 结构式为:O=C=O。答案为: 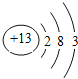 ;
;![]() ;O=C=O;
;O=C=O;
(2)Na与Mg均属于同种周期元素,由于核电核数Na![]() Mg,故半径Na
Mg,故半径Na![]() Mg,因此,答案为: Na>Mg;
Mg,因此,答案为: Na>Mg;
(3)因为非金属性Cl![]() S,故酸性:高氯酸大于硫酸,答案为: H2SO4 ;
S,故酸性:高氯酸大于硫酸,答案为: H2SO4 ;
(4)因为非金属性S>P,故H2S更易制备,因此,答案为: H2S;
(5)氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,氢氧化铝难溶,不能拆,水为氧化物不能拆,离子反应方程式为: Al(OH)3+OH-=AlO2-+2H2O,答案为: Al(OH)3+OH-=AlO2-+2H2O;
(6)H、O和Na形成的共价化合物为水,离子化合物为过氧化钠、氧化钠、氢氧化钠等,答案为: H2O、Na2O


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
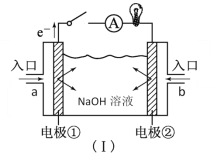
【题目】(1)如图装置(Ⅰ)为以NaOH溶液为电解质溶液的氢氧燃料电池。装置(Ⅰ)中a和b为气体进口,其中a口进入的是(填名称)____,写出电极②发生反应的电极反应式______。
(2)将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图的装置:(以下均假设反应过程中溶液体积不变)。
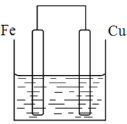
①铁片上的电极反应式为_____。
②溶液中的铜离子移向____(填铁电极或铜电极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法不正确的是
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法不正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2min的平均速率v(Z)=2.0×10-3 mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前:v(逆)<v(正)
C. 该温度下此反应的平衡常数:K=1.44
D. 保持其他条件不变,起始时向容器充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,c(Z)=0.024 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙醇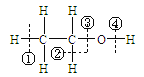 在化学反应中断键位置说法错误的是 ( )
在化学反应中断键位置说法错误的是 ( )
A. 乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应。
B. 乙醇与钠反应,在④位置断裂,对比钠与水反应,乙醇比水更难失去氢离子。
C. 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应。
D. 乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.01000 mol·L-1的盐酸滴定0.01000 mol·L-1NaA溶液20.00mL。滴定曲线如图所示,下列说法错误的是( )
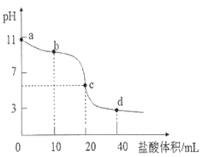
A. 当滴入盐酸以后,c(HA)+c(A-)<0.01000 mol·L-1
B. b点溶液中微粒浓度大小关系为:c(HA)>c(A-)>c(Cl -)>c(OH-)>c(H+)
C. c点时,溶液中微粒浓度关系为:c(Na+)<c(HA)+2c(A-)
D. d点时,溶液中微粒浓度存在关系:c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示,根据判断出的元素回答问题:
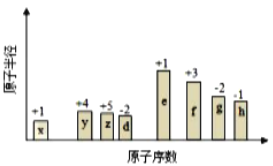
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式____________________。
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如图所示:
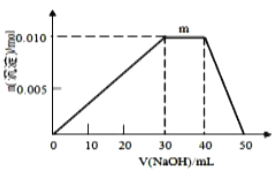
①R中存在的化学键有________________。
②写出m点反应的而离子方程式________________________________。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后产生沉淀的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物X的结构简式为 ,下列有关叙述不正确的是 ( )
,下列有关叙述不正确的是 ( )
A. 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
B. X在一定条件下能与FeCl3溶液发生显色反应
C. X在一定条件下能发生消去反应和酯化反应
D. X的化学式为C10H10O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a曲线表示一定条件下可逆反应:X(g)+Y(g) ![]() 2Z(g)+W(g) △H<0 的反应过程中X的转化率和时间的关系,若使a曲线变为b曲线,可采取的措施是
2Z(g)+W(g) △H<0 的反应过程中X的转化率和时间的关系,若使a曲线变为b曲线,可采取的措施是

A. 加入催化剂 B. 增大Y的浓度
C. 降低温度 D. 增大体系压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com