
| A. | 离子键是阴阳离子之间的静电引力 | |
| B. | 只有原子才满足核内质子数和核外电子数相等 | |
| C. | 离子化合物中一定有金属元素 | |
| D. | 氕、氘、氚互为氢元索的同位素,H2O、D2O和T2O是不同的分子 |
分析 A.阴阳离子之间的作用力包括静电引力和排斥力;
B.原子呈电中性;
C.铵盐也为离子化合物,但都由非金属元素构成;
D.H2O、D2O和T2O是同种物质.
解答 解:A.离子键是由离子形成的,即阴阳离子之间通过静电作用(既有吸引也有排斥)形成离子键,故A错误;
B.原子呈电中性,原子核外电子数与质子数相等,而离子肯定不等,故B正确;
C.铵盐也为离子化合物,但都由非金属元素构成,则离子化合物中不一定有金属元素,故C错误;
D.H2O、D2O和T2O都同种元素构成的化合物,为同种物质,故D错误.
故选B.
点评 本题综合考查离子键、原子构成以及同位素等知识,为高频考点,侧重于基本概念的理解以及学生的分析能力的考查,注意相关基础知识的积累,难度不大,易错点为D.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇的分子式:CH3OCH3 | B. | 氯化氢分子的电子式: | ||
| C. | 乙烯的结构式:CH2CH2 | D. | 中子数为8的碳原子:614C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 性质(氯水的漂白性);原因(氯气的强氧化性) | |
| B. | 性质(明矾用来净水);原因(Al3+水解生成Al(OH)3胶体,具有吸附性) | |
| C. | 性质(苯燃烧有浓黑的烟);原因(苯分子中含碳量较高) | |
| D. | 性质(加热铝箔,熔化的铝不滴落);原因(氧化膜熔点高,包在熔化的铝外面) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2与O2不再化合生成SO3 | B. | SO2、O2、SO3的分子数之比是2:1:2 | ||
| C. | SO3的合成速率与分解速率相等 | D. | 增大压强,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数为7的元素的最高化合价为+4价 | |
| B. | 114号元素位于第七周期ⅣA族 | |
| C. | 位于同一主族的甲、乙两种元素,甲的原子序数为m,则乙的原子序数可能为m+4 | |
| D. | 位于同一周期的甲、乙两种元素,甲位于第ⅠA族,原子序数为m,乙位于第ⅢA族,则乙的原子序数可能为m+19 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
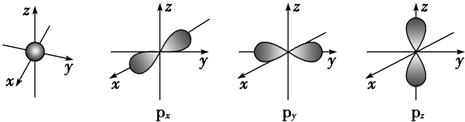
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有四瓶失去标签的溶液,知道他们是乙醛、乙酸、乙醇和甲酸,用新制的Cu(OH)2悬浊液可以将四种溶液一一鉴别 | |
| B. | 已知苹果酸的结构简式为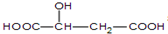 ,则该物质可发生氧化反应、酯化反应、缩聚反应,与HOOC-CH2-CH(OH)-COOH互为同分异构体 ,则该物质可发生氧化反应、酯化反应、缩聚反应,与HOOC-CH2-CH(OH)-COOH互为同分异构体 | |
| C. | 按系统命名法,化合物 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| D. | 等物质的量的乙炔、乙醛、(HO)CH2-CH2(OH)完全燃烧时的耗氧量不相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com