
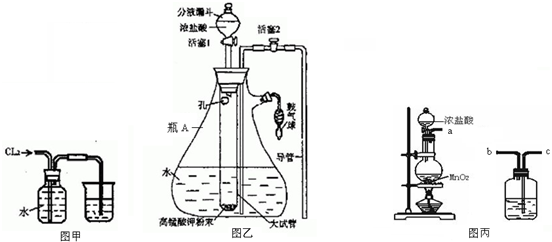
分析 (1)氯水中的次氯酸不稳定易分解为盐酸和氧气;
(2)氯气有毒,直接排放能引起空气污染,可以和强碱反应,用碱液吸收;
(3)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、水和氯气;制取的氯气中含有水蒸气,氯化氢,先通过盛有饱和食盐水的洗气瓶除去氯化氢,再通过盛有浓硫酸的洗气瓶除去水;
(4)制取的氯气中含有水蒸气,氯化氢,先通过盛有饱和食盐水的洗气瓶除去氯化氢,再通过盛有浓硫酸的洗气瓶除去水;
(5)增大压强可以增大氯气的溶解度;一次加入太多的盐酸会使得产生的氯气的量多,出现很大的压强;
(6)根据大气压强原理来寻找排出液体的方法.
解答 解:(1)氯水中的次氯酸不稳定易分解为盐酸和氧气,2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,所以氯水久置会因为次氯酸分解而失效,
故答案为:2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑;
(2)氯气有毒,多余的氯气不排放到空气中去,氯气可以和强碱氢氧化钠反应来吸收氯气,
故答案为:氢氧化钠溶液;吸收过量的氯气;
(3)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、水和氯气,方程式:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;制取的氯气中含有水蒸气,氯化氢,先通过盛有饱和食盐水的洗气瓶除去氯化氢,再通过盛有浓硫酸的洗气瓶除去水,洗气时应长进短出,所以正确的顺序为:acbcb;
故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;acbcb;
(4)制取的氯气中含有水蒸气,氯化氢,先通过盛有饱和食盐水的洗气瓶除去氯化氢,再通过盛有浓硫酸的洗气瓶除去水;
故答案为:饱和食盐水,除去氯化氢;浓硫酸,除去水蒸气;
(5)图乙装置能在较短时间内得到饱和氯水,除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是氯气在瓶内产生较大的压强,增大了氯气的溶解度,分液漏斗中的盐酸应分数次加入试管内,若一次加入太多的盐酸,和高锰酸钾反应产生的氯气量太多,会导致瓶内压强过大会使瓶A的橡皮塞弹开,
故答案为:氯气在瓶内产生较大的压强,增大了氯气的溶解度;在瓶内产生过多的氯气,瓶内压强过大会使瓶A的橡皮塞弹开.
(6)配制氯水完成后,不必拆卸装置即可从瓶A中取用少量氯水,打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气,瓶内压强增大,会将液体从A瓶中排出,
故答案为:打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气.
点评 本题考查了氯气的实验室制备,明确氯气性质以及制取原理是解题关键,属于综合知识的考查,难度大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1LC2H5OH燃烧后生成的CO2分子数约为$\frac{{N}_{A}}{11.2}$ | |
| B. | 电解食盐水水时,当产生22.4LH2时,电路中转移的电子数为2NA | |
| C. | 标准状况下,11.2LCH4和C2H4混合气体中含有碳原子的数目为2NA | |
| D. | NH3易溶于水,3.4gNH3溶于1LH2O,溶液中氮原子总数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com