
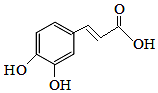
| A. | 能发生加聚反应 | |
| B. | 能与碳酸钠溶液反应 | |
| C. | 1 mol咖啡酸最多能与3 mol NaOH反应 | |
| D. | 1 mol咖啡酸最多能与 3 mol Br2反应 |
分析 有机物含有酚羟基,可发生取代、氧化和显色反应,含有碳碳双键,可发生加成、加聚以及氧化反应,含有羧基,具有酸性,可发生取代反应.
解答 解:A.含有碳碳双键,可发生加聚反应,故A正确;
B.含有羧基,具有酸性,可与碳酸钠溶液反应,故B正确;
C.有机物中含有2个酚羟基和1个羧基,都具有酸性,则1mol咖啡酸最多能与3molNaOH反应,故C正确;
D.有机物中含有2个酚羟基,可被取代的H原子共有3个,分子中含有碳碳双键,可与溴发生加成反应,在1mol咖啡酸最多能与4molBr2反应,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于考查学生化学知识的应用能力,题目难度不大,注意把握有机物官能团的性质.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:选择题
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关溶液中离子浓度关系叙述正确的是( )
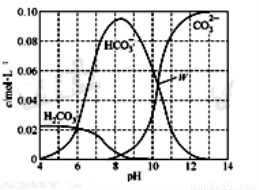
A.W点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)
B.pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)<0.1mol·L-1
C.pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-)
D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向容积固定的容器甲和带有活塞的定压容器乙中分别通入2mol SO2和1mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡.则下列说法正确的是( )
向容积固定的容器甲和带有活塞的定压容器乙中分别通入2mol SO2和1mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡.则下列说法正确的是( )| A. | 平衡时,两容器内SO3的浓度必定相等 | |
| B. | 平衡时,混合气体中的SO3的体积分数甲比乙高 | |
| C. | SO2的转化率乙容器内比甲容器内高 | |
| D. | 反应后的相同时间内,甲容器中的反应速率大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强或降低温度,平衡常数K都增大 | |
| B. | 其它条件相同,向容器中只加入2molZ,能建立完全相同的平衡状态 | |
| C. | 平衡时,平衡常数K=36a(mol/L)-1 | |
| D. | 某时刻X、Y、Z物质的量分别是0.3mol,1mol和1.1mol,反应正向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4NH3+5O2═4NO+6H2O | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2NaHCO3═Na2CO3+H2O+CO2 | D. | Cl2+2NaBr═2NaCl+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
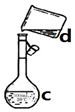 (1)现需配制0.1mol/LNaOH溶液500mL,装置是某同学转移溶液的示意图
(1)现需配制0.1mol/LNaOH溶液500mL,装置是某同学转移溶液的示意图查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石与醋酸反应制取二氧化碳:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯乙酸与足量氢氧化钠溶液共热:CH2ClCOOH+OH-→CH2ClCOO-+H2O | |
| C. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| D. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO${\;}_{3}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com