
【题目】下列反应属于氧化还原反应的是( )
A.CaCO3+2HCl=CaCl2+H2O+CO2↑
B.Na2O+H2O=2NaOH
C.CaCO3=CaO+CO2↑
D.Mg+2HCl=MgCl2+H2↑
科目:高中化学 来源: 题型:
【题目】常温下,可以用铁或铝制的容器贮存浓硫酸,下列叙述中,错误的是
A.浓硫酸具有强还原性
B.贮存浓硫酸的容器要密封,因为浓硫酸容易吸收空气中的水蒸气
C.浓硫酸可以使硫酸铜晶体由蓝色变为白色
D.常温下,浓硫酸可以使铁或铝钝化,生成一层致密的氧化膜,阻止反应继续进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过一步反应不能直接完成的是( )
①N2→NO2②S→SO2 ③NH3→NO④NO→HNO3⑤CuSO4→Cu(NO3)2⑥SiO2→H2SiO3 .
A.①⑥
B.④⑤
C.①④
D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用MgCl2、AlCl3混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
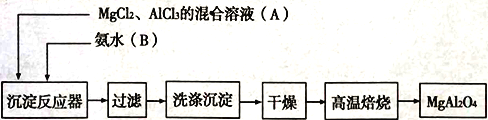
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应容器中加入________(填“A”、或“B”),再滴加另一反应物。
(2)实验室利用氯化铵和熟石灰反应制取氨气,写出反应的化学方程式________________________。
(3)判断流程中沉淀是否洗净所用的试剂是______________;高温焙烧时,用于盛放固体的仪器名称是__________________。
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

①写出装置A 中发生反应的离子方程式________________________。
②装置B中盛放饱和NaCl溶液,该装置的主要作用是__________;F中试剂的作用是__________;
用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为__________。
③实验步骤:如图连接装置后,先__________(填实验操作),再装药品,然后点燃______(填“ A” 或“C” )处酒精灯,当________(填实验现象)时,再点燃另一处酒精灯。
④写出装置G 中发生反应的离子方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过一步反应不能直接完成的是( )
①N2→NO2②S→SO2 ③NH3→NO④NO→HNO3⑤CuSO4→Cu(NO3)2⑥SiO2→H2SiO3 .
A.①⑥
B.④⑤
C.①④
D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》中记载“烧酒非古法也,自元时始创其法。用浓酒和糟入甑,蒸令气上,用器承取其露。”这里用到的方法可用于分离( )
A.碳酸钙和硝酸钾B.碘单质和氯化钠C.四氯化碳和水D.乙醇和乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅单质及其化合物应用很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:![]()
①写出由纯SiHCl3制备高纯硅的化学反应方程式。
②整个制备过程必须严格控制无水、无氧。SiHCl3遇水剧烈反应生成H2SiO3、
HCl和另一种物质,写出配平的化学反应方程式;H2
还原SiHCl3过程中若混有O2 , 可能引起的后果是。
(2)下列有关硅材料的说法正确的是( )。
A.单质硅化学性质稳定,但可以被强碱溶液腐蚀
B.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D.光导纤维的主要成分是SiO2
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入盐酸,
振荡。写出实验现象并给予解释(用化学方程式说明)。
(4)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是________(填字母)。
A.高温结构陶瓷
B.生物陶瓷
C.导电陶瓷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O (g)CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= , 该反应为反应(填吸热或放热).若改变条件使平衡向正反应方向移动,则平衡常数(填序号)
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是 .
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO (g) 和H2O (g) 分别通入到体积为2L的恒容密闭容器中,进行反应CO (g)+H2O (g)CO2(g)+H2(g),得到如表三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO2 | CO | |||
A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
C | 1000 | 1 | 2 | c | d | t |
①实验B中平衡时H2O (g)的物质的量是 .
②通过计算可知,CO的转化率实验A实验B(填“大于”、“等于”或“小于”).
③若实验C中达到平衡所需时间 t3(填“大于”、“等于”或“小于”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列各组物质:①甲烷和乙烯;②乙烯和乙醇;③苯和乙炔;④甲苯和邻二甲苯;⑤丙烯和2﹣丁烯,只要总质量一定,各组中两种物质不论以任何比例混合,完全燃烧时生成水的质量也总是定值的是( )
A.②⑤
B.②③④⑤
C.③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com