
【题目】下列与阿伏加德罗常数的值(NA)有关的说法中,不正确的是
A. 18g H218O与D2O的混合物中,中子数为9NA
B. 标准状况下,22.4 L Cl2与NaOH溶液完全反应时转移电子的数为NA
C. 1L0.1 mol L-1NH4NO3溶液中加稀氨水,溶液呈中性时NH![]() 数为0.1NA
数为0.1NA
D. 4.6 gC2H6O中含有的C—H数目为0.6NA
【答案】D
【解析】
A、H218O与D2O的摩尔质量均为20g/mol,故18gH218O与D2O的物质的量均为0.9mol,而两者中均含10个中子,故0.9mol混合物中含9mol中子即9NA个,选项A正确;
B、标准状况下,22.4LCl2的物质的量为0.1mol,与足量NaOH溶液反应的化学方程式Cl2+2NaOH=NaCl+NaClO+H2O,反应中,1mol氯气自身发生氧化还原反应,电子转移数为NA,选项B正确;
C.将1mol NH4NO3溶于稀氨水中使溶液呈中性,则溶液中存在电荷守恒:c(H+)+ c(NH4+)= c(NO3-)+ c(OH-),溶液呈中性,则铵根离子浓度等于硝酸根离子浓度,溶液体积相等,则氨根离子数目等于硝酸根离子数,为1mol,溶液中NH4+数目为NA,选项C正确;
D.该有机物可能是乙醇也可能是乙醚,4.6g该有机物的物质的量是0.1mol,如果是乙醇,所含C-H键数目一定为0.5NA,如果是乙醚,含有的C-H键数目一定为0.6NA,如果是乙醇和乙醚的混合物,则含有的C-H键数目介于二者之间,选项D不正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】28g CO气体在1mol的氧气中燃烧后,所得的气体通过足量Na2O2固体中充分反应后,下列说法不正确的是( )
A. CO与氧气反应,只消耗了0.5mol氧气
B. 充分反应后Na2O2固体质量增加了28 g
C. 通过以上两步反应后余下氧气物质的量为0.5mol
D. 若2gH2替代 28g的CO发生上述反应,则Na2O2固体质量增加了2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用A和B为原料合成E的路线如下。已知B的分子式为C2H2O3 ,可发生银镜反应且具有酸性,回答下列问题:

(1)E中含氧官能团的名称为_____________________。
(2)A的名称为_________。写出B 发生银镜反应的化学方程式_________________。
(3)C→D反应的化学方程式为____________,D→E的反应类型是_____________。
(4)写出符合下列条件的C的所有同分异构体(不考虑立体异构)的结构简式___________。
①属于羧酸类芳香化合物 ②核磁共振氢谱中出现4组峰
(5)设计由乙酸为起始原料制备OHC-COOH 的合成路线(无机原料任选):
CH3COOH ClCH2COOH ________________________________________。
ClCH2COOH ________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=-1200KJ/mol,温度不同(T2>T1)其他条件相同时,下列图像正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋酸钠( NaBiO3 )是一种难溶于水的强氧化剂,在钢铁工业中常用作锰元素的分析测定。某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3,SiO2等杂质)制备铋酸钠,其流程如下:

请回答下列问题:
(1)为了提高“浸取”中原料的浸出率,可以采取的措施是_________________(写一种即可) 。
(2)“浸取”时通常加入FeCl3溶液和浓盐酸,向其中加入过量浓盐酸的目的是_____,“滤渣”的成份是____________(填化学式)。
(3)“沉淀”反应的离子方程式为__________________________________________________;
(4)“沉淀”操作时,用氨水调节pH至6,通过计算说明,此时溶液中的Bi3+是否完全沉淀:____________________(已知:Bi(OH)3的溶度积Ksp=3×10-32) 。
(5)“焙烧”除了采用最佳的质量比、合适的温度外,你认为还需要控制的条件是________。
(6)已知,在酸性溶液中NaBiO3将Mn2+氧化为MnO4-。请出该反应的离子方程式:__________。
(7)某辉铋矿中铋元素的质量分数为20.90%,若100吨该辉铋矿完全用于生产,共得到25.00吨NaBiO3,则产率是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物可将废水中苯酚的化学能直接转化为电能,装置如图所示。电池工作时,下列说法正确的是

A. a极为正极,发生氧化反应
B. b极的电极反应式为:2NO3-+12H++10e-===N2↑+6H2O
C. 中间室的Cl-向右室移动
D. 左室消耗苯酚 (C6H5OH) 9.4 g时,用电器流过2.4 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用容量瓶配制溶液时,由于操作不当,会引起误差。下列情况会使所配溶液浓度偏低的是( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A. ①②⑤B. ①③⑤C. ③④⑤D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某0.2L无土栽培用的营养液中含有KCl、K2SO4、NH4Cl三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:

(1)该营养液中K2SO4的物质的量浓度为____mol·L-1,含KCl的质量为____。
(2)该营养液中NH4Cl的物质的量为____。
(3)将该营养液加水稀释,稀释过程中NH![]() 的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则V1=____,V2=___。
的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则V1=____,V2=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TMB由碳氢氮三种元素组成,其相对分子质量为240,是一种新型指纹检测的色原试剂,已在逐步取代强致癌物联苯胺和其他致癌性的联苯胺衍生物应用于临床化验法医检验刑事侦破及环境监测等领域。某研究小组欲利用燃烧法测定TMB的分子式(氮元素转化为N2)实验装置如图所示。回答下列问题:
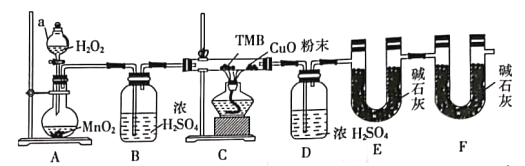
(1)实验装置两处用到装有碱石灰的干燥管,其中F处的目的是______________________。仪器a的名称是___________。
(2)将足量双氧水置于a中,圆底烧瓶中装入MnO2固体,按图连接好装置。
①A中发生反应的化学方程式为______________________。
②待B、D处导管口有均匀气泡时,再点燃C处酒精灯,原因是______________________。
(3)装置C中CuO粉末的作用为_________________________________。
(4)该实验___________(填“需要”或“不需要”)尾气处理,其原因是____________________。
(5)理想状态下,将4.80gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60g,E增加14.08g,则TMB的分子式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com