
由乙烯和乙醇蒸汽组成的混合气体中,若碳元素的质量分数为72%,则氧元素的质量分数为( )
|
| A. | 32.00% | B. | 16.00% | C. | 14.22% | D. | 2.14% |
| 元素质量分数的计算. | |
| 专题: | 有机物分子组成通式的应用规律. |
| 分析: | 乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的分子式看作C2H4•H2O,混合物可以看作C2H4、H2O的混合物,根据碳元素的质量百分含量可计算出C2H4的质量分数,进而计算的水质量分数,计算氧元素的质量百分含量. |
| 解答: | 解:乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的分子式看作C2H4•H2O,混合物可以看作C2H4、H2O的混合物, 已知:ω(C)=72%,则ω(C2H4)= 则ω(H2O)=1﹣84%=16%, 所以:ω(O)=16%× 故选:C. |
| 点评: | 本题考查元素质量分数的计算,题目难度不大,注意利用分子式的转化,将乙醇的分子式可作C2H4•H2O. |


科目:高中化学 来源: 题型:
以乙炔或苯为原料可合成有机酸H2MA,并进一步合成高分子化合物PMLA。
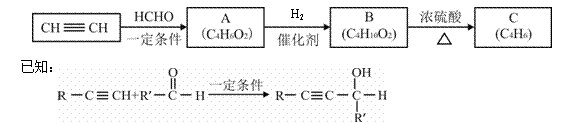 I.用乙炔等合成烃C。
I.用乙炔等合成烃C。
(1)A分子中的官能团名称是 、
(2)A的结构简式是
A的一种同分异构体属于乙酸酯,其结构简式是 。
(3)B转化为C的化学方程式是 ;
其反应类型是 反应。
II.用烃C或苯合成PMLA的路线如下。

已知:

(4)1 mol有机物H与足量NaHCO3溶液反应生成标准状况下的CO2 44.8 L,H有顺反异构,其反式结构简式是
(5)E的结构简式是
(6)G与NaOH溶液在加热条件下反应的化学方程式是
(7)H的核磁共振氢谱呈现 个吸收峰。
(8)聚酯PMLA有多种结构,写出由H2MA制PMLA的化学方程式(任写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物X的分子式为C3H6O2.X在酸性条件下与水反应,生成的有机物Y和Z.Y在铜催化下被氧化为W,Z和W能发生银镜反应.
(1)X和Z的名称为:X ,Z .
(2)写出下列反应的化学方程式:
Y与浓硫酸的混合物共热发生消去反应 ,W与新制Cu(OH)2、NaOH混合溶液共热发生的反应 .
查看答案和解析>>
科目:高中化学 来源: 题型:
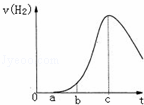
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L﹣1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图的坐标曲线来表示,下列推论错误的是( )
|
| A. | t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液 |
|
| B. | t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
|
| C. | t>c产生氢气的速率降低主要是因为溶液中c(H+)降低 |
|
| D. | t=c时反应处平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
N2+3H2 2NH3是目前工业上合成氨的反应,下列关于该反应的说法正确的是( )
2NH3是目前工业上合成氨的反应,下列关于该反应的说法正确的是( )
|
| A. | 增加N2的浓度能加快反应速率 |
|
| B. | 降低体系温度能加快反应速率 |
|
| C. | 使用催化剂不影响反应速率 |
|
| D. | 若反应在密闭容器中进行,N2和H2能100%转化为NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com