
【题目】(1)用系统命名法给下列有机物命名:
①![]() __;
__;
②(CH3)3COH__;
(2)相对分子质量为114,其一氯代物只有一种的链烃的结构简式__,该物质的名称为__。
【答案】2,4—二甲基—3—乙基—3—己烯 2—甲基—2—丙醇 (CH3)3CC(CH3)3 2,2,3,3—四甲基丁烷
【解析】
(1)①该有机物为烯烃,选取含有碳碳双键的最长碳链为主链,该有机物主链为己烯,然后根据烯烃的命名原则写出其名称;
②(CH3)3COH为醇,羟基在2号C,主链为丙醇,甲基在2号C,根据醇的命名原则写出其名称;
(2)根据链烃的通式及相对分子量进行讨论,然后确定该链烃的分子式,再根据一氯代物只有一种确定该有机物的结构简式,最后利用系统命名法进行命名。
(1)①![]() ,含有碳碳双键的最长碳链含有6个C,主链为己烯,选取含有支链最多的碳链为主链,从距离碳碳双键最近、支链编号最小右端开始编号,碳碳双键在3号C,在2、4号C各含有1个甲基,在3号C含有1个乙基,该有机物名称为:2,4二甲基3乙基3己烯;
,含有碳碳双键的最长碳链含有6个C,主链为己烯,选取含有支链最多的碳链为主链,从距离碳碳双键最近、支链编号最小右端开始编号,碳碳双键在3号C,在2、4号C各含有1个甲基,在3号C含有1个乙基,该有机物名称为:2,4二甲基3乙基3己烯;
②(CH3)3COH主链为丙醇,羟基在2号C,在2号C含有1个甲基,该有机物名称为:2-甲基-2-丙醇;
(2)相对分子质量为114,常见的链烃有烷烃、烯烃和炔烃等,根据![]() =8…2可知,该有机物为烷烃,其分子式为C8H18,一氯代物只有一种的链烃,说明该有机物分子中的氢原子位置只有1种,满足该条件的结构简式为:(CH3)3CC(CH3)3,该有机物主链为丁烷,在2、3号C各含有2个甲基,该有机物的名称为:2,2,3,3四甲基丁烷。
=8…2可知,该有机物为烷烃,其分子式为C8H18,一氯代物只有一种的链烃,说明该有机物分子中的氢原子位置只有1种,满足该条件的结构简式为:(CH3)3CC(CH3)3,该有机物主链为丁烷,在2、3号C各含有2个甲基,该有机物的名称为:2,2,3,3四甲基丁烷。


科目:高中化学 来源: 题型:
【题目】下列实验操作或装置符合实验要求的是()
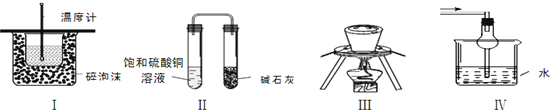
A.装置Ⅰ可用于测定中和热
B.装置Ⅱ装置放置一段时间后,饱和![]() 溶液中不出现蓝色晶体
溶液中不出现蓝色晶体
C.装置Ⅲ中的石英坩埚可用于熔化氢氧化钠
D.装置Ⅳ可用于吸收易溶于水的尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.能够使品红试液褪色的气体一定是![]()
B.常温下,铁、铝不与浓硫酸反应,因此可以用铁、铝容器贮存运输浓硫酸
C.硝酸铵受热易分解爆炸,实验室常加热氯化铵与氢氧化钙的混合物制备氨气
D.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. SO2![]() CaSO3
CaSO3![]() CaSO4
CaSO4
B. Fe![]() Fe2O3
Fe2O3![]() FeCl3
FeCl3
C. HCl(aq) ![]() Cl2
Cl2![]() Ca(ClO)2
Ca(ClO)2
D. Cu2(OH)2CO3![]() CuO
CuO![]() CuCl2(aq)
CuCl2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院化学所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛用途,其生产过程的部分流程如下:
![]()
下列有关叙述不合理的是
A. 纳米四氧化三铁可分散在水中,它与FeCl3溶液的分散质直径相当
B. 纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
C. 在反应①中环丙胺的作用可能是促进氯化铁水解
D. 反应②的化学方程式是6FeOOH +CO=2Fe3O4+3H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将200mLH2SO4和Fe2(SO4)3的混合溶液分成两等份,向其中一份中加入足量铁粉,充 分反应后测得固体质量减少3.36g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干燥、称量,得到23.3g白色沉淀。请计算:
(1)原溶液中c(SO42﹣)=_____。
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A在标准状况下的密度为1.25gL﹣1,以A和水煤气(CO、H2)为原料在一定条件 下可获得有机物B、C、D、E,其相互转化关系如图。已知B是CO与H2以物质的量之比为 1:1 反应的产物,E为有浓郁香味、不易溶于水的油状液体。
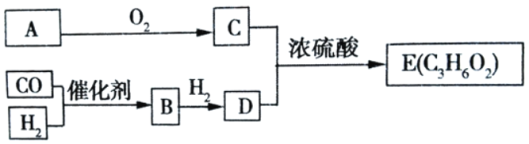
请回答:
(1)有机物C种含有的官能团名称是_____。
(2)C+D→E的反应类型是_____。
(3)有机物B在一定条件下转化为D的化学方程式是_____。
(4)下列说法不正确的是_____。
A.有机物D与金属钠反应比水与金属钠反应要剧烈
B.有机物C、D、E可用饱和碳酸钠溶液鉴别
C.实验室制备E时,浓硫酸主要起氧化作用
D.有机物 B、C均能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,向三个初始体积为1L的密闭容器中按表所示投料,发生反应N2(g)+3H2(g)2NH3(g)△H<0,达到平衡时,下列说法错误的是
容器编号 | 容器类型 | 起始物质的量 | 反应物的转化率 | 平时时 | ||
|
|
| ||||
Ⅰ | 恒温恒容 | 1 | 3 | 0 |
|
|
Ⅱ | 绝热恒容 | 0 | 0 | 2 |
| a |
Ⅱ | 恒温恒压 | 1 | 3 | 0 |
| b |
A.平衡时NH3的物质的量:a>1.2,b>1.2
B.容器I、II中平衡常数关系:K(I)>K(II)
C.a1+a2<1
D.若起始时向容器A中充入lmolN2(g)、0.4molH2(g)、0.4molNH3(g),此时平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、[Al(OH)4]-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示。下列说法正确的是

A. BC段是OH-与盐酸反应
B. 反应后最终溶液中的溶质只有NaC1
C. 原溶液中含有CO32-与[Al(OH)4]-的物质的量之比为3:4
D. 原溶液中一定含有的离子是Na+、OH-、SiO32-、SO42-、[A1(OH)4]-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com