
| |||||||||||||||||||||
 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
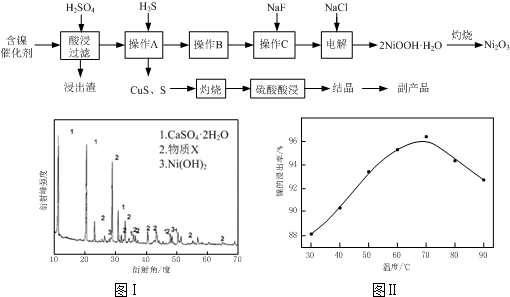
| �������� | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 | 7.7 |
| ������ȫ��pH | 3.7 | 9.7 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����������Ϊ1L�ĺ�������a��b��ģ��һ̼��ѧ�ϳɼ�ȩ���ϳɹ����е�ԭ���ɱ�ʾΪCO��g��+H2��g��?HCHO��g������������a��ʹ�ô�������������CO��H2�����ʵ�����ͬ����Ϊ1mol���Իش��������⣺
�����������Ϊ1L�ĺ�������a��b��ģ��һ̼��ѧ�ϳɼ�ȩ���ϳɹ����е�ԭ���ɱ�ʾΪCO��g��+H2��g��?HCHO��g������������a��ʹ�ô�������������CO��H2�����ʵ�����ͬ����Ϊ1mol���Իش��������⣺| ʵ���� | T���棩 | n��CO��/n��H2�� | p��Mpa�� | ||||
| �� | 150 |
|
0.1 | ||||
| �� | 150 150 |
|
5 | ||||
| �� | 350 |
|
5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ʵ�� ��� |
ʵ�� �¶�/�� |
0.1mol/LNa2S2O3��Һ�����/mL | H2O�� ���/mL |
0.1mol/LH2SO4��Һ�����/mL | ���� ʱ��/s |
| �� | 25 | 5 | 5 | 2 | / |
| �� | 25 | 5 | 6 | 1 | / |
| �� | 35 | 5 | 5 | V | / |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com