
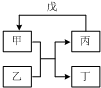
 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,满足如图所示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,满足如图所示转化关系的是( )| 甲 | 乙 | 丙 | 戊 | |
| A | Na2O2 | CO2 | O2 | Na |
| B | Fe | H2O | Fe2O3 | H2 |
| C | MgO | 盐酸 | MgCl2 | NaOH |
| D | CuSO4 | Zn | Cu | 稀H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据反应甲+乙→丙+丁,丙+戊→甲分析,将四个选项中的各物质代入,结合物质的性质判断这两个反应是否能发生,如果能发生,则正确,否则错误.
解答 解:A、2Na2O2+2CO2=2Na2CO3+O2,2 Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2,所以能实现转化,故A正确;
B、3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O,所以能实现转化,故错误;
C、丙氯化镁与氢氧化钠反应生成氢氧化镁而不是氧化镁,故C错误;
D、丙铜与戊稀硫酸不反应,故D错误;
故选A.
点评 本题考查物质之间的化学反应,明确物质的性质是解本题关键,注意铁和水蒸气反应生成四氧化三铁而不是氧化铁,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 含有泥沙的浑水,静置一会儿水沙分离,可取得上层的清水 | |
| B. | 农村“扬谷”分离饱满的谷粒和干瘪的谷壳 | |
| C. | 建筑工地上用铁筛把大小不同的沙粒分开 | |
| D. | 淘米除去米中混有的小沙粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
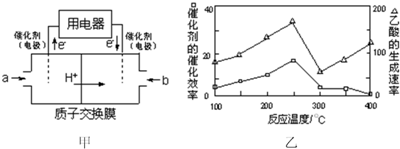
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在18 g18O2中含有NA个氧原子 | |
| B. | 在氮原子中,质子数为7而中子数不一定为7 | |
| C. | D${\;}_{2}^{16}$O中,质量数之和是质子数之和的两倍 | |
| D. | Cl-的结构示意图为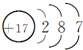 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
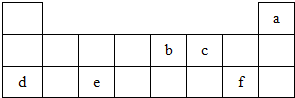
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应 | |
| B. | 淀粉、纤维素水解的最终产物均为葡萄糖 | |
| C. | 由甲烷的氯代物有4种,可推知乙烷的氯代物有6种 | |
| D. | 天然油脂没有固定的熔点和沸点,所以天然油脂是混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的气态氢化物的水溶液显酸性 | |
| B. | X的原子半径小于Y | |
| C. | Z的最外层电子数比Y多 | |
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaHSO4溶液中滴Ba(OH)2溶液.恰好使溶液呈中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| B. | 镁粉撒入NH4Cl溶液:Mg+2H+═Mg2++H2↑ | |
| C. | 过量SO2通入Ca(ClO)2溶液中:ClO-+SO2+H2O═HSO3-+HClO | |
| D. | 向FeI2溶液中通入等量氯气:2I-+C12═I2+2Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com