
| A. | 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ | |
| B. | 因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3═2NaIO3+Cl2不能发生 | |
| C. | 反应3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是3:1 | |
| D. | 在反应CaH2+2H2O═Ca(OH)2+2H2↑中,水作氧化剂 |
分析 A.观察K的焰色反应应透过蓝色的钴玻璃;
B.置换反应I2+2NaClO3═2NaIO3+Cl2能发生,Cl得到电子,I失去电子;
C.NO2为氧化剂、还原性;
D.水中H元素的化合价由+1价降低为0.
解答 解:A.观察K的焰色反应应透过蓝色的钴玻璃,则灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,不能确定是否含K+,故A错误;
B.置换反应I2+2NaClO3═2NaIO3+Cl2能发生,Cl得到电子,I失去电子,则Cl2的氧化性强于I2的氧化性,故B错误;
C.NO2为氧化剂、还原性,由电子、原子守恒可知,3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是1:2,故B错误;
D.水中H元素的化合价由+1价降低为0,则水为氧化剂,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意从元素的化合价角度分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1.8g18O2分子与1.8g18O3分子中含有的中子数不同 | |
| B. | 7.8gNa2S和7.8g Na2O2中含有的阴离子数目均为0.1NA | |
| C. | 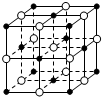 23.4 g NaCl晶体中含有0.1NA个如图所示的结构单元 | |
| D. | 含16 g氧原子的二氧化硅晶体中含有的δ键数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 $\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )
$\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )| A. | 取代反应、加成反应、取代反应 | B. | 取代反应、取代反应、加成反应 | ||
| C. | 氧化反应、加成反应、加成反应 | D. | 氧化反应、加成反应、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
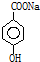 ②NaHCO3 ③Al ④
②NaHCO3 ③Al ④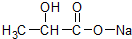 ⑤Al2(SO4)3.
⑤Al2(SO4)3.| A. | ①③ | B. | ③⑤ | C. | ①②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 酸性高锰酸钾溶液应装在酸式滴定管中,原因是酸性高锰酸钾能氧化橡胶 | |
| C. | 植物油和裂化汽油都能使溴水褪色,原理是不同的 | |
| D. | 明矾能够用于净水,是因为明矾的溶液是酸性的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
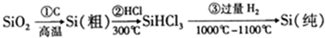 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 步骤①的化学方程式为:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | 步骤①②③中每生成或反应1mol Si,转移2mol电子 | |
| C. | 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应 | |
| D. | SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

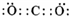 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
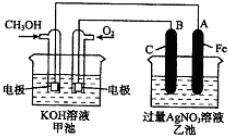
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com