
【题目】喹啉(![]() )是治疗新冠肺炎的药物氯喹的基础原料,其合成路线如下:
)是治疗新冠肺炎的药物氯喹的基础原料,其合成路线如下:
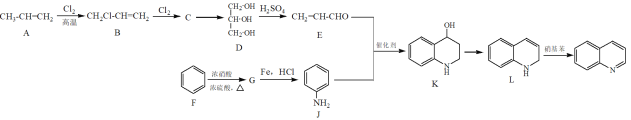
下列有关说法正确的是
A.C→D的反应条件为NaOH水溶液,加热
B.可以用溴水来检验化合物E中的碳碳双键
C.F→G和G→J的反应类型分别为取代反应和还原反应
D.与喹啉互为同分异构体,且含有碳碳双键和氰基(-CN)的芳香族化合物共有4种
【答案】AC
【解析】
CH3-CH=CH2与Cl2在高温下发生取代反应生成CH2Cl-CH=CH2,CH2Cl-CH=CH2与Cl2发生加成反应生成的C是CH2Cl-CHCl-CH2Cl,C与NaOH的水溶液共热发生取代反应生成D:CH2OH-CH(OH)CH2OH,D与浓硫酸共热,发生反应生成E:CH2=CH-CHO,F是苯,苯与浓硫酸、浓硝酸混合加热发生取代反应生成的G是硝基苯:![]() ,G在Fe、HCl存在条件下发生还原反应生成J:
,G在Fe、HCl存在条件下发生还原反应生成J:![]() ,然后根据题意分析解答。
,然后根据题意分析解答。
A. B是CH2Cl-CH=CH2,B与Cl2发生加成反应生成的C是CH2Cl-CHCl-CH2Cl,C与NaOH的水溶液共热,发生取代反应生成D,A正确;
B. 溴水具有强氧化性,不仅可以与碳碳双键发生加成反应,也能将醛基氧化为羧基,醛基的存在对碳碳双键的检验构成干扰,因此不能只用溴水来检验E中的碳碳双键,B错误;
C. F→G是取代反应,而G→J是还原反应,C正确;
D. 喹啉分子式是C9H7N,与喹啉互为同分异构体,且含有碳碳双键和氰基(-CN)的芳香族化合物有![]() 、
、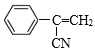 、
、![]() 、
、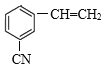 、
、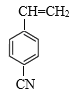 共有5种,D错误;
共有5种,D错误;
故答案选AC。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】ClO2和NaClO2均具有漂白性,工业上用ClO2气体制NaClO2的工艺流程如图所示。
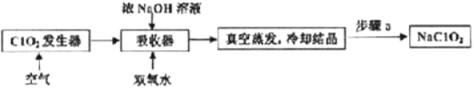
下列说法不正确的是
A.步骤a的操作包括过滤、洗涤和干燥
B.吸收器中生成NaClO2的离子方程式为2ClO2+H2O2=2ClO2-+2H+ +O2↑
C.工业上将ClO2气体制成NaCIO2固体,其主要目的是便于贮存和运输
D.通入的空气的目的是驱赶出ClO2,使其被吸收其充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示,下列有关说法不正确的是( )
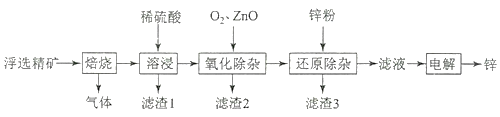
A.滤渣1的成分是SiO2 , 滤渣2的成分是Fe(OH)3
B.焙烧过程中主要反应的化学方程式为2ZnS+3O2![]() 2ZnO+2SO2
2ZnO+2SO2
C.溶液中的Cd2+可用锌粉除去,反应的离子方程式为Zn+Cd2+=Zn2++Cd
D.若不通入氧气,其后果是无法除去杂质Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物F(![]() )是有机合成的中间体。现以甲苯为原料合成F的路线如图所示。
)是有机合成的中间体。现以甲苯为原料合成F的路线如图所示。

已知:①R-CN![]() R-COOH
R-COOH
②
回答下列问题:
(1)A→B的反应试剂是___。
(2)B→C反应的化学方程式为___,反应类型是___。D→E的反应类型是___。
(3)D中含氧官能团的名称是___。
(4)G是F的同系物,比F多一个碳原子,其苯环上含两个取代基的同分异构体有___种(不考虑立体异构)。其中核磁共振氢谱有六组峰,且峰面积之比为1:1:1:2:2:3的有机物结构简式为___。
(5)结合以上合成路线及相关信息,设计由苯合成苯酚的合成路线___。(用合成流程图表示,并注明反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是原子序数为1~19的元素第一电离能的变化曲线(其中部分元素第一电离能已经标出数据)。结合元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列有关问题。
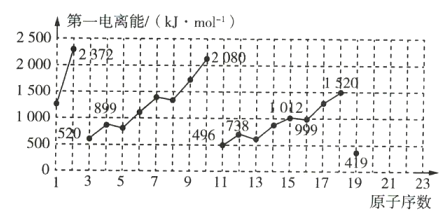
(1)碱金属元素中Li、Na、K的第一电离能分别为 _____________ ![]() 、 _____________
、 _____________ ![]() 、 _____________
、 _____________ ![]() 。
。
(2)同主族中不同元素的第一电离能变化的规律为: _____________ ,碱金属元素这一变化的规律与碱金属的活泼性的关系是 _____________ 。
(3)钙元素的第一电离能的数值范围为 _____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图,下列对该物质的叙述中正确的是

A.该有机物能发生取代反应、氧化反应和消去反应
B.1mol该有机物最多可与2molNaOH发生反应
C.该有机物可以与溴的四氯化碳溶液发生加成反应使之褪色
D.该有机物有3个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(1)H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol-1
O2(g)=H2O(g) ΔH1=akJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol-1
(3)H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol-1
O2(g)=H2O(l) ΔH3=ckJ·mol-1
(4)2H2(g)+O2(g)=2H2O(l) ΔH4=dkJ·mol-1;下列关系式中正确的是( )
A.a<c<0B.2a=b<0C.b>d>0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________________________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______。
(4)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K______1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡____移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为__________(填“正反应方向”“逆反应方向”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g) ![]() C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。下列分析不正确的是( )
C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。下列分析不正确的是( )
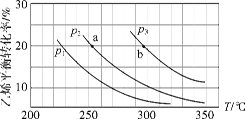
A.乙烯气相直接水合反应的H<0
B.图中压强的大小关系为:p1>p2>p3
C.图中a点对应的平衡常数K =![]()
D.达到平衡状态a、b所需要的时间:a>b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com