
| 元素代号 | 原子结构或元素性质 |
| X | 最高正价=|最低负价| |
| Y | 原子核及核外各层电子的排布情况如图: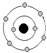 |
| Z | 原子结构示意图: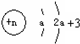 |
| L | 原子半径为同周期主族元素中最大 |
| M | 其原子序数比L大2 |
 ,Y原子核外电子数为8,则Y为O元素,X的原子序数小于Y,所以X为C元素;
,Y原子核外电子数为8,则Y为O元素,X的原子序数小于Y,所以X为C元素;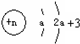 ,K电子层最多排列2个电子,所以a=2,L电子层电子数为7,则Z原子核外有9个电子,为F元素;
,K电子层最多排列2个电子,所以a=2,L电子层电子数为7,则Z原子核外有9个电子,为F元素;

 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:不详 题型:单选题
| | a | b | c |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | CH2=CH2 | CH3CH2OH | CH3CHO |
 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 |
| B.Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物高 |
| C.Z、W、R最高价氧化物对应水化物的酸性强弱顺序是R>W>Z |
| D.Y分别与Z、W、R以两种元素组成的常见化合物有5种,且它们晶体类型相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
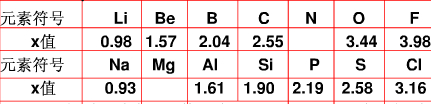
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 293116 |
| A.②③⑥⑧ | B.①④⑤⑦ | C.①③⑥⑧ | D.①④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X元素气态氢化物的水溶液呈酸性 |
| B.X能形成化学式为NaXO3的含氧酸钠盐 |
| C.X原子的最外层电子数和核电荷数不可能为偶数 |
| D.X元素常见单质的化学式为X2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 520 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5] | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 178 |
| A.X原子中质子数为17,中子数为8 |
| B.X原子中质子数等于中子数 |
| C.X原子中质子数为8,中子数为9 |
| D.X原子中质子数为17,质量数为8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com