


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ģ½Ī÷ÉĻČÄ֊ѧø߶žµŚŅ»“ĪŌĀæ¼£ØÖŲµć°ą£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ä»ÆĪŖ·ÅČȵĻÆѧ·“Ó¦µÄŹĒ(””””)

A£®H2O(g)===H2O(l)””¦¤H£½£44.0 kJ/mol
B.2HI(g)===H2(g)£«I2(g)””¦¤H£½£«14.9 kJ/mol
C.ŠĪ³É»Æѧ¼üŹ±¹²·Å³ö862 kJÄÜĮæµÄ»Æѧ·“Ó¦
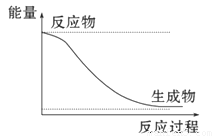
D£®ÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾µÄ»Æѧ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ģŗž±±Ź”ø߶žµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ä»ÆĪŖ·ÅČȵĻÆѧ·“Ó¦µÄŹĒ(””””)
A£®H2O(g)===H2O(l)””¦¤H£½£44.0 kJ/mol
B£®2HI(g)===H2(g)£«I2(g)””¦¤H£½£«14.9 kJ/mol
C£®ŠĪ³É»Æѧ¼üŹ±¹²·Å³ö862 kJÄÜĮæµÄ»Æѧ·“Ó¦
D£®ÄÜĮæ±ä»ÆČēĻĀĶ¼ĖłŹ¾µÄ»Æѧ·“Ó¦

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ģÕć½Ź”øßŅ»ĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ä»ÆĪŖ·ÅČȵĻÆѧ·“Ó¦µÄŹĒ
A£®H2O£Øg£©==H2O(l) ¦¤H=-44.0 kJ/mol
B£®2HI(g)==H2(g)+I2(g) ¦¤H=+14.9 kJ/mol
C£®ŠĪ³É»Æѧ¼üŹ±¹²·Å³öÄÜĮæ862 kJµÄ»Æѧ·“Ó¦
D£®ÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾µÄ»Æѧ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com