
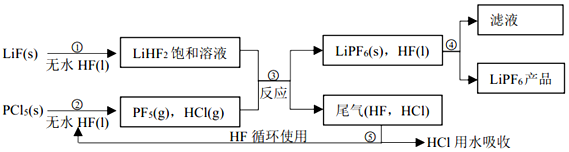
���� ��1��������Ŀ�е����̿��Կ���������+Һ���������+������Һ��������ˮHF�������Ƿ�Ӧ����ܼ�����������Ҫ�ɷ��к��ж������裬�ܺ�HF������Ӧ��
��2������Ԫ����ɿ�֪��������ֱ���H3PO4��HF��
��3������Һ��Ͳ�����Һ�������ù��˷��룬HF���Ӽ京��������е����HCl���ɲ������������룮
��� �⣺��1��������Ŀ�е����̿��Կ���������+Һ���������+������Һ��������ˮHF�������Ƿ�Ӧ����ܼ�����������Ҫ�ɷ��к��ж������裬�ܺ�HF������Ӧ����ѧ����ʽΪSiO2+4HF�TSiF4��+2H2O���ʴ�Ϊ����Ӧ��ܼ���SiO2+4HF�TSiF4��+2H2O��
��2��������Ŀ�е���Ϣ��PF5����ˮ�⣬�����Ϊ�����ᡱ�������Ԫ����ɿ�֪��������ֱ���H3PO4��HF�����Է�Ӧ�ķ���ʽΪPF5+4H2O�TH3PO4+5HF��
�ʴ�Ϊ��PF5+4H2O�TH3PO4+5HF��
��3���ڢܲ�������ǹ��壨LiPF4��s������Һ�壨HF��l���������Բ��ù��˵ķ���������β����HF��HCl���������ö��߷е�IJ��죨HF����֮�������������з��룬���Բ�����������
�ʴ�Ϊ�����ˣ�������
���� ����Ϊ����ѧ�����⣬�����Ǹ߿��еij������ͣ������е��Ѷȵ����⣮�����ۺ���ǿ���漰�����ƶϡ������ᴿ������ʽ��д����ѧ�����֪ʶ��ע�����������Ϣ��ʹ�ã����ض�ѧ��ʵ�������������ͽ��ⷽ����ָ��������������ѧ���淶���Ͻ���ʵ����ƺ�����������


 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Al��NaOH��Һ��Ӧ�����ӷ���ʽΪ2Al+2NaOH+2H2O=2NaAlO2+3H2����
��Al��NaOH��Һ��Ӧ�����ӷ���ʽΪ2Al+2NaOH+2H2O=2NaAlO2+3H2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ��Ʒ������/g | NaOH��Һ�����/mL | ���������/L |
| �� | 7.4 | 40.00 | 1.68 |
| �� | 14.8 | 40.00 | 3.36 |
| �� | 22.2 | 40.00 | 1.12 |
| �� | 37.0 | 40.00 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
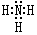 ��D������Һ̬X�з�����������A2C�ķ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ2Na+2NH3=2NaNH2+H2����
��D������Һ̬X�з�����������A2C�ķ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ2Na+2NH3=2NaNH2+H2����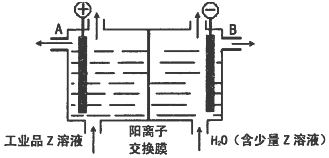
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������Ԫ�ص����ʻ�ṹ��Ϣ���£�
��������Ԫ�ص����ʻ�ṹ��Ϣ���£�| Ԫ�ر�� | �����Ϣ |
| X | �ؿ��к������Ľ���Ԫ�أ�Ԫ�����Ϊ+3�ۣ� |
| Y | ԭ�������������ǵ��Ӳ�����2����������������X������������2���� |
| Z | ͬ��������Ԫ����ԭ�Ӱ뾶��С�������µ��ʳ�Һ̬�� |
| M | �ܴӺ�ˮ����ȡ�Ľ���Ԫ�أ����ʿ��ڵ����������̼��ȼ�գ� |
 ������Ԫ������������Ӧ��ˮ���������ǿ���ǣ�д����ʽ��Mg��OH��2��Ԫ����Ԫ�ط��ű�ʾ����ͬ������
������Ԫ������������Ӧ��ˮ���������ǿ���ǣ�д����ʽ��Mg��OH��2��Ԫ����Ԫ�ط��ű�ʾ����ͬ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe��MnO2 | B�� | C��FeS | C�� | Si��FeO | D�� | CuO��Ag2S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
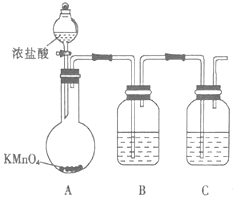

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
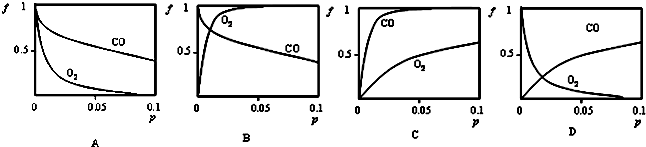

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̪ݼ���ķ��ӣ�ֱ��Ϊ1.3��10-9m����ˮ���γɵķ�ɢϵ�ܲ��������ЧӦ | |
| B�� | ��������ϸ�ڲ����Լ�ƿ���� | |
| C�� | ճ�������ʵ��Թܿ��þƾ�ϴ�� | |
| D�� | ���ع��͡�������Ƶÿ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com