
【题目】在一定温度下,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡状态的标志是( )
2C(g)达到平衡状态的标志是( )
A.C的生成速率与C的分解速率相等
B.A、B、C的分子数之比为1:3:2
C.单位时间生成nmolA,同时生成3nmolB
D.A、B、C的浓度相等
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,△H 能正确表示物质的标准燃烧热的是
A.CO(g)+ ![]() O2(g)=CO2(g) △H =-283 kJ/mol
O2(g)=CO2(g) △H =-283 kJ/mol
B.C(g)+ ![]() O2(g)=CO(g) △H =-110.5 kJ/mol
O2(g)=CO(g) △H =-110.5 kJ/mol
C.H2(g)+ ![]() O2(g)=H2O(g) △H =-248.1 kJ/mol
O2(g)=H2O(g) △H =-248.1 kJ/mol
D.2C2H2(g)+5O2(g)=2H2O(l)+4CO2(g) △H =-2300 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在amL浓度为cmol·L-1的AgNO3溶液中加入一定体积的pH=1的盐酸时,恰好使溶液中Ag+完全沉淀,此时得到pH=2的溶液100 mL(设反应前后溶液体积变化忽略不计),则c的值是
A.0.0020B.0.011 C.0.11D.0.22
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压条件下,把30mL甲烷和氧气的混合气体点燃,冷却至常温,测得气体的体积为16mL,则原混合气体中甲烷和氧气的体积比?____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两元素可形成AB型离子化合物,且阴、阳离子具有相同的电子数.A、B的单质均能与水发生剧烈反应,反应中A单质做还原剂,B单质做氧化剂,则下列表述正确的是![]()
A.B元素原子的电子排布式为1s22s22p63s23p5
B.化合物AB的电子式为![]()
C.化合物AB的电子式为![]()
D.A与水反应的离子方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁是由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 离子中的两种组成,可以发生如图转化,下列说法不正确的是
离子中的两种组成,可以发生如图转化,下列说法不正确的是![]()
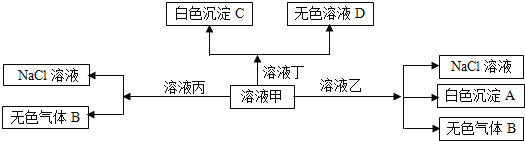
A.在甲中滴加丁可能发生反应:![]()
B.溶液丙中还可以大量共存的离子有:![]() 、
、![]() 、
、![]()
C.白色沉淀A可能溶解在溶液D中
D.甲为![]() ,乙为
,乙为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增。已知:
①W的原子序数为29,其余的均为短周期主族元素;
②T原子所处的周期数、族序数分别与其原子序数相等;
③X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同;
④Z的基态原子价电子排布为ns2npn+2;
⑤在该元素所在周期中,Q的基态原子的第一电离能最小;
⑥R的单质常温常压下是气体,其基态原子的M层上有1个未成对的p电子;
(1)X、Y、Q三种元素的电负性由大到小的顺序是___(用元素符号表示)。
(2)Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是___。
(3)W的基态原子的核外电子排布式为___。
(4)T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为XT2Z,分子空间构型为平面三角形,则该分子中心原子采取___杂化,1molM分子中σ键和π键的个数比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式表示正确的是 ( )
A.碳酸钙与醋酸溶液反应:CaCO3 +2H+ =Ca2++ CO2 ↑+H2O
B.苯酚钠溶液和少量CO2反应: 2C6H5O +CO2 +H2O=2C6H5OH +CO32
C.溴乙烷与氢氧化钠溶液共热:C2H5Br+OH ![]() C2H5OH+Br
C2H5OH+Br
D.用银氨溶液检验乙醛的醛基:CH3CHO + 2Ag(NH4)2OH ![]() CH3COO- + NH4+ +3NH3 + 2Ag↓+H2O
CH3COO- + NH4+ +3NH3 + 2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )
A. 它的系统名称是2,4-二甲基-4-戊烯
B. 它的分子中至少有5个碳原子在同一平面上
C. 它与甲基环己烷(![]() )互为同分异构体
)互为同分异构体
D. 该有机物与氢气完全加成后的产物的一氯取代产物共有4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com