
| 元素 | 结构或性质信息 |
| M | M的一种单质是自然界最硬的物质 |
| Q | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
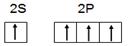 ,请判断对错,并加以解释
,请判断对错,并加以解释  电子式___________
电子式___________  寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.任一主族元素均由非金属元素和金属元素组成 |
| B.第n周期第n主族的元素可能是金属元素,也可能是非金属元素 |
| C.第n周期有(8-n)种非金属元素(1<n≤7,包括稀有气体) |
| D.同种元素的不同粒子,它们的电子层数可能不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2(ax+by)+60 | B.ax+by+60 | C.(ax+by)/2+60 | D.ay+bx+60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.n=m+16 | B.n=m+6 | C.n=m+30 | D.n=m+31 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 水 | 四氯化碳 |
| 溴 | 黄→棕 | 橙→橙红 |
| 碘 | 深黄→褐 | 紫→深紫 |
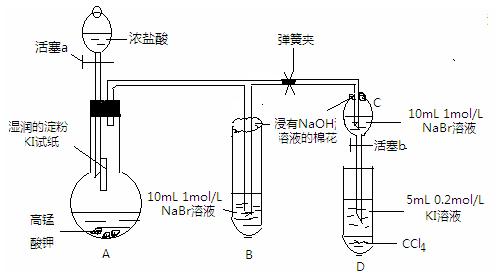
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
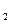 B中溶解性由大到小的顺序为 (填化学式),其原因是 。
B中溶解性由大到小的顺序为 (填化学式),其原因是 。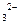 中的B的杂化类型为 ,空间结构为 ,与BD
中的B的杂化类型为 ,空间结构为 ,与BD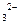 互为等电子体且含C、D两元素的微粒的化学式为 。
互为等电子体且含C、D两元素的微粒的化学式为 。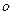 键与
键与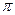 键的个数比为 ,该分子的VSERR模型 。
键的个数比为 ,该分子的VSERR模型 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com