

 (2)D和B互为同分异构体,且其苯环上的一氯代物只有两种,D不与NaHCO3反应,能与Na和NaOH反应,等质量的D消耗的Na,NaOH的物质的量之比为2:3,请写出两种D的结构简式为
(2)D和B互为同分异构体,且其苯环上的一氯代物只有两种,D不与NaHCO3反应,能与Na和NaOH反应,等质量的D消耗的Na,NaOH的物质的量之比为2:3,请写出两种D的结构简式为 或
或
 .
. 分析 根据题中信息可知,有机官能团的酸性大小为-COOH>H2CO3>酚-OH>H2O>醇-OH,
(1)根据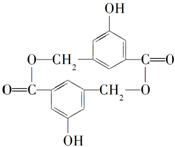 水解可得B知,B的结构为
水解可得B知,B的结构为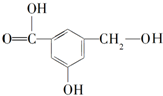 ,在B的各官能团中,-COOH、酚-OH、醇-OH能与钠反应,-COOH、酚-OH能与NaOH反应,-COOH能与NaHCO3反应,据此答题;
,在B的各官能团中,-COOH、酚-OH、醇-OH能与钠反应,-COOH、酚-OH能与NaOH反应,-COOH能与NaHCO3反应,据此答题;
(2)D和B互为同分异构体,且其苯环上的一氯代物只有两种,D不与NaHCO3反应,说明不含有羧基,能与Na和NaOH反应,等质量的D消耗的Na,NaOH的物质的量之比为2:3,则说明D中有两个羟基,另外还有一个酯基,据此答题;
(3)根据题中信息,1molC能和1mol钠完全反应,说明C中有一个羟基,A的分子式为C7H6O3,1mol的A、C完全燃烧,消耗氧气的质量相等,则C为分子式可以为C6H6O,据此写C的结构;
解答 解:据题中信息可知,有机官能团的酸性大小为-COOH>H2CO3>酚-OH>H2O>醇-OH,
(1)根据 水解可得B知,B的结构为
水解可得B知,B的结构为 ,在B的各官能团中,-COOH、酚-OH、醇-OH能与钠反应,-COOH、酚-OH能与NaOH反应,-COOH能与NaHCO3反应,每molB可以消耗3molNa、2molNaOH、1molNaHCO3,所以等物质的量的B分别与Na,NaOH,NaHCO3充分反应,消耗Na,NaOH,NaHCO3的物质的量之比为3:2:1,
,在B的各官能团中,-COOH、酚-OH、醇-OH能与钠反应,-COOH、酚-OH能与NaOH反应,-COOH能与NaHCO3反应,每molB可以消耗3molNa、2molNaOH、1molNaHCO3,所以等物质的量的B分别与Na,NaOH,NaHCO3充分反应,消耗Na,NaOH,NaHCO3的物质的量之比为3:2:1,
故答案为:3:2:1;
(2)D和B互为同分异构体,且其苯环上的一氯代物只有两种,D不与NaHCO3反应,说明不含有羧基,能与Na和NaOH反应,等质量的D消耗的Na,NaOH的物质的量之比为2:3,则说明D中有两个羟基,另外还有一个酯基,则D为 或
或 ,
,
故答案为: 或
或 ;
;
(3)根据题中信息,1molC能和1mol钠完全反应,说明C中有一个羟基,A的分子式为C7H6O3,1mol的A、C完全燃烧,消耗氧气的质量相等,则C为分子式可以为C6H6O,所以C的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断及结构与性质,为高频考点,把握习题中的信息推断物质及官能团与性质的关系为解答的关键,综合性较强,题目难度中等.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
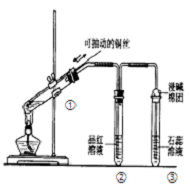
| A. | 装置①能控制反应的发生和结束 | |
| B. | 若将反应后②的试管取下,在通风橱中加热,会产 生刺激性气味的气体,溶液呈红色 | |
| C. | ③中石蕊溶液变红色 | |
| D. | 为确认CuSO4生成,向①中加水,观察溶液颜色 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高二上期中化学试卷(解析版) 题型:选择题
下列实验操作能达到测量要求的是( )
A. 用托盘天平称量25.21 g氯化钠
B. 用10 mL量筒量取7.50 mL稀硫酸
C. 用25 mL滴定管量取14.86 mL溶液
D. 用广泛pH试纸测得溶液的pH为4.2
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 分类方法在化学学科的发展中起了非常重要的作用.如图是某反应在密闭容器中反应前后的分子状况示意图,“
分类方法在化学学科的发展中起了非常重要的作用.如图是某反应在密闭容器中反应前后的分子状况示意图,“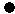 ”和“
”和“ ”分别表示不同的原子.对此反应的分类一定不正确的是( )
”分别表示不同的原子.对此反应的分类一定不正确的是( )| A. | 置换反应 | B. | 氧化还原反应 | C. | 放热反应 | D. | 化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体 | |
| B. | 溶剂蒸发的速度越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大 | |
| C. | 用倾析法分离时,将烧杯中的上层清液用玻璃棒引流到另一容器内,即可使沉淀与清液分离 | |
| D. | 用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
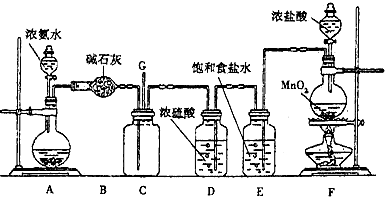
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取11.70 g食盐 | |
| B. | 用量筒量取12.36 mL盐酸 | |
| C. | 用酸式滴定管量取21.20 mL 0.10 mol•L-1的H2SO4溶液 | |
| D. | 测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,点在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应过程中,一定有新物质生成 | |
| B. | 化学反应过程中,一定有化学键的断裂和形成 | |
| C. | 化学反应过程中,一定有能量的变化 | |
| D. | 如果某化学反应的△H和△S均小于0,则该反应一定能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com