
| A�� | �ۢ� | B�� | �ڢܢ� | C�� | �ڢۢܢ� | D�� | �٢ڢۢܢ� |
���� �ٲ�ͬ�ǽ���Ԫ��֮�����γɼ��Լ���ͬ�ַǽ���Ԫ��֮�����γɷǼ��Լ�������������IJ��غϵķ���Ϊ���Է��ӣ�������������غϵķ���Ϊ�Ǽ��Է��ӣ�
�ڲ�ͬ�ǽ���Ԫ��֮�����γɼ��Լ���ͬ�ַǽ���Ԫ��֮�����γɷǼ��Լ�������������IJ��غϵķ���Ϊ���Է��ӣ�������������غϵķ���Ϊ�Ǽ��Է��ӣ�
�۵ȵ�����Ľṹ���ƣ�
�ܱ�ͪ���Ӽ�û�������
�����ǻ���������ڷ�������������ǻ���������ڷ��Ӽ������
��� �⣺�ټ��Է���һ�����м��Լ����Ǽ��Է��Ӳ�һ�����зǼ��Լ����������̼��ֻ���м��Լ����ṹ�Գ��ǷǼ��Է��ӣ��ʴ���
�ڼ��Է����п��ܺ��зǼ��Լ�������������к���O-O�Ǽ��Լ������ڼ��Է��ӣ��Ǽ��Է����п��ܺ��м��Լ����������̼��ֻ���м��Լ����ṹ�Գ��ǷǼ��Է��ӣ��ʴ���
�۵ȵ�����Ľṹ���ƣ�N2O��CO2�ǻ�Ϊ�ȵ����壬������̼�ĽṹʽΪO=C=O����N2O�ĽṹʽΪ��N=N=O�����ÿ�����Ӿ�����2���� ����������ԭ�Ӿ�Ϊsp�ӻ�������ȷ��
�ܱ�ͪ���Ӽ�û���������ͪ���ӵ���Է����������ڶ��飬���Ա�ͪ�ķе���ڶ��飬������أ��ʴ���
�ݶ��ǻ����������γɷ���֮������������ǻ��������γɷ�����������������ǻ���������ۡ��е�ȶ��ǻ�������ĵͣ�����ȷ��
��ѡA��
���� ���⿼�鹲�ۼ����������������ʵ����ʵ�Ӱ�죬��ȷ�����ҪӰ�����ʵ����������ǽ����Ĺؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
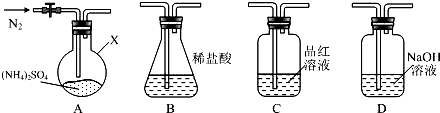
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
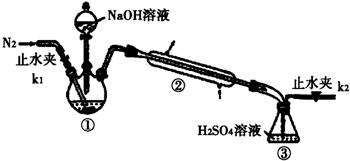
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al | B�� | Na | C�� | Zn | D�� | Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 168O��178O��188O����ͬλ�� | |
| B�� | N60��N2��Ϊͬϵ�� | |
| C�� | O2��O3��H2��D2��H218O��H216O����Ϊͬ�������� | |
| D�� | CH2O2��C2H4O2��C3H6O2��C4H8O2��Ϊͬϵ��Ҷ�����������Ҳ��Ϊͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
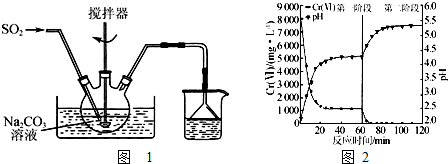
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
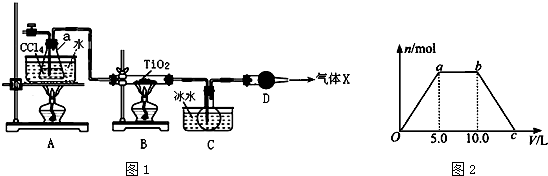
| ���� | �۵�/�� | �е�/�� | ���� |
| CCl4 | -23 | 76.8 | ��TiCl4���� |
| TiCl4 | -25 | 136 | ����ʪ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܢݢޢ� | B�� | �ܢݢߢ� | C�� | �ۢܢݢ� | D�� | �ۢܢݢߢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com