
����Ŀ����仯ѧ���������о����̿�(��Ҫ�ɷ���MnO2)�Ĺ����У�������Ũ�����ϼ��ȣ������˻���ɫ���塣
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
(2)��Ӧ����������_______���ѧʽ������Ԫ�صĻ��ϼ�________����������������������������������17.4 g MnO2�������ɱ�״����Cl2�������_______L��ת�Ƶ��ӵ����ʵ�����______mol��
(3)�ô˷�Ӧ�Ƶõ������г�����_______��Ҫ�ռ������﴿����������Ӧʹ��������ͨ��װ��_______��_______��ϴ��ƿ�����ռ���
���𰸡�MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O MnO2 ���� 4.48 0.4 HCl��ˮ���� �����Ȼ�����Һ Ũ����
MnCl2+Cl2��+2H2O MnO2 ���� 4.48 0.4 HCl��ˮ���� �����Ȼ�����Һ Ũ����
��������
(1)MnO2��Ũ�����ϼ��ȣ�����������ԭ��Ӧ����������
(2)�ڷ�Ӧ�У�Ԫ�ػ��ϼ����ߣ�ʧȥ���ӣ���������ԭ����Ԫ�ػ��ϼ۽��ͣ��õ����ӣ������������������ݷ���ʽ������ת����ϵ������MnO2���������㷴Ӧ������Cl2�����ʵ�����������V=n��Vm���������ڱ�״���µ����������Ԫ�ػ��ϼ������������ڷ�Ӧ�����е���ת�������������ת�Ƶ����ʵ�����
(3)����������лӷ��ԣ���Ϸ�Ӧ��Ҫ�ڼ��������·��������л��е����ʣ����ӵ�˳�����ȳ�ȥ�������ʣ������
(1)MnO2��Ũ�����ϼ��ȣ������˻���ɫCl2����Ӧ�ķ���ʽΪ��MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
(2)�ڸ÷�Ӧ�У�MnԪ�ػ��ϼ��ɷ�ӦǰMnO2�е�+4�۱�Ϊ��Ӧ��MnCl2�е�+2�ۣ����ϼ۽��ͣ��õ����ӣ�����MnO2����������17.4 g MnO2�����ʵ���Ϊn(MnCl2)=17.4 g��87 g/mol= 0.2 mol�����ݷ���ʽMnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��֪��ÿ��1 mol MnO2��Ӧ�������1 mol Cl2����0.2 mol MnO2��Ӧ����Cl2�����ʵ�����0.2 mol���ڱ�״���µ����V=n��Vm=0.2 mol��22.4 L/mol=4.48 L���ɷ���ʽ��֪��1 mol MnO2��Ӧ��ת��2 mol ���ӣ���0.2 mol MnO2��Ӧ��ת��0.4 mol ���ӣ�
MnCl2+Cl2��+2H2O��֪��ÿ��1 mol MnO2��Ӧ�������1 mol Cl2����0.2 mol MnO2��Ӧ����Cl2�����ʵ�����0.2 mol���ڱ�״���µ����V=n��Vm=0.2 mol��22.4 L/mol=4.48 L���ɷ���ʽ��֪��1 mol MnO2��Ӧ��ת��2 mol ���ӣ���0.2 mol MnO2��Ӧ��ת��0.4 mol ���ӣ�
(3)��Ũ������������̻�ϼ�����ȡ������Ũ������лӷ��ԣ���Ӧ����Һ�н��У������ȡ�õ��������к�������HCl��ˮ������Ҫ�ռ������﴿����������Ӧʹ������ͨ��װ�б����Ȼ���ˮ��ϴ��ƿ��ȥ����HCl��Ȼ����ͨ��Ũ������и������ٽ����ռ���


 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ������������������裨![]() ����ˮ��һ�������£�������
����ˮ��һ�������£�������![]() ��Ӧ���������塣����˵������ȷ����
��Ӧ���������塣����˵������ȷ����
A. ![]() ��̼Ԫ�صĻ��ϼ�Ϊ+2
��̼Ԫ�صĻ��ϼ�Ϊ+2
B. �÷�Ӧ�IJ���֮һ������![]()
C. ��1mol![]() ���뷴Ӧʱ��ת��
���뷴Ӧʱ��ת��![]()
D. ������0.1mol![]() �ķ�ˮ����������Ҫ���ı�״����
�ķ�ˮ����������Ҫ���ı�״����![]() �����Ϊ5.6L
�����Ϊ5.6L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������м������ʣ��뽫����������пո��ڣ�
A��C60��ʯī
B��126C��136C
C�������������
D��CH3CHO ��![]()
E�������ʮ����
F���Ҵ����Ҷ���
�ٻ�Ϊͬϵ�����_________________��
�ڻ�Ϊͬ���칹�����_____________��
�ۻ�Ϊͬλ�ص���________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״����1molij����ȫȼ��ʱ������89.6LCO2����֪0.1mol���������״����4.48LH2�ӳɣ�������Ľṹ��ʽ��
A.CH3CH=CHCH3B.CH3C��CCH3
C.CH3CH2CH=CH2D.CH2=CHCH=CHCH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH��MgCl2��AlCl3���ֹ�����ɵĻ������������ˮ��,����1.16g��ɫ����,����������Һ������1.00mol��L-1HCl��Һ,����HCl��Һ����������ɳ����Ĺ�ϵ��ͼ��ʾ��
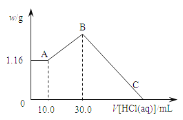
�Իش�:
��1��A������Ļ�ѧʽΪ______��
��2��д��A����B�㷢����Ӧ�����ӷ���ʽ_______��
��3����ԭ�������AlCl3������____��NaOH�����ʵ���____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС������ȡ�������������ͼ��ʾװ�ã����������ɿ�ѡ�ã���
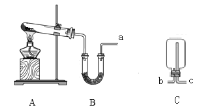
(1)A���ư����Ļ�ѧ����ʽ��____________________________________��
(2)B��Ӧװ___________��������____________��
(3)�ռ�����ʱ��Bװ�õ�a��Ӧ����Cװ�õ�___________������b������c�����ڣ�֤�������Ѽ����IJ�����������______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���ˮ��Һ��1 mol ClOx��(x��0��1��2��3��4)������(kJ)��Դ�С��ͼ��ʾ�������й�˵����ȷ����( )
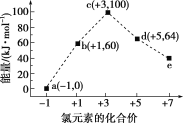
A.e��ClO3��
B.b��a��c��Ӧ�Ļ��Ϊ60 kJ��mol��1
C.a��b��c��d��e��c���ȶ�
D.b��a��d��Ӧ���Ȼ�ѧ����ʽΪ3ClO��(aq)=2Cl��(aq)��ClO3��(aq)����H����116 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���F������ij����Ѫҩ���Ʊ�����ҵ����F��һ��·��ͼ���£�����H��FcCl3��Һ�ܷ�����ɫ��Ӧ����
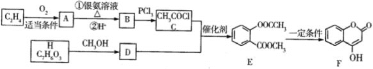
�ش��������⣺
(1) A��������_____,E�еĹ�����������_______��
(2) B��C�ķ�Ӧ������___, F�ķ���ʽΪ_______��
(3) H�Ľṹ��ʽΪ__.
(4) E��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ___��
(5)ͬʱ��������������D��ͬ���칹�干��_____�֣�д���˴Ź���������5�������ʵĽṹ��ʽ___��
���Ƿ����廯����
������NaHCO3��Һ��Ӧ��������FeCl3��Һ������ɫ��Ӧ
��l mol���������Ʒ�Ӧʱ���ɵõ�1molH2
(6)��2-�ȱ��ᡢ����Ϊԭ���Ʊ��۱�ϩ�ᱽ������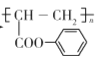 ��,д���ϳ�·��ͼ�����Լ���ѡ��___��
��,д���ϳ�·��ͼ�����Լ���ѡ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C(s)+CO2(g)![]() 2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
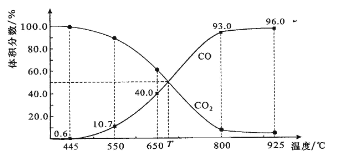
��֪�������ѹ��P����=������ѹ��P�������������������˵����ȷ����
A. 550��ʱ��������������壬������ ����С��ƽ�ⲻ�ƶ�
B. 650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25.0%
C. T��ʱ��������������CO2��CO��ƽ�����淴Ӧ�����ƶ�
D. 925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��KP=24.0P��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com