
”¾ĢāÄæ”æ298 KŹ±£¬ŌŚ2 L¹Ģ¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśæÉÄę·“Ó¦£ŗ2NO2(g) ![]() N2O4(g)””¦¤H£½£a kJ/mol(a>0)”£N2O4µÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£“ļĘ½ŗāŹ±£¬N2O4µÄÅضČĪŖNO2µÄ2±¶£¬Čō·“Ó¦ŌŚ398 K½ųŠŠ£¬Ä³Ź±æĢ²āµĆn(NO2)£½0.6 mol£¬n(N2O4)£½1.2 mol£¬Ōņ“ĖŹ±£¬ĻĀĮŠ“󊔹ŲĻµÕżČ·µÄŹĒ(””””)
N2O4(g)””¦¤H£½£a kJ/mol(a>0)”£N2O4µÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£“ļĘ½ŗāŹ±£¬N2O4µÄÅضČĪŖNO2µÄ2±¶£¬Čō·“Ó¦ŌŚ398 K½ųŠŠ£¬Ä³Ź±æĢ²āµĆn(NO2)£½0.6 mol£¬n(N2O4)£½1.2 mol£¬Ōņ“ĖŹ±£¬ĻĀĮŠ“󊔹ŲĻµÕżČ·µÄŹĒ(””””)

A. v(Õż)>v(Äę)
B. v(Õż)<v(Äę)
C. v(Õż)£½v(Äę)
D. v(Õż)”¢v(Äę)“󊔹ŲĻµ²»Č·¶Ø
”¾“š°ø”æB
”¾½āĪö”æŹŌĢā·ÖĪö£ŗøł¾ŻĶ¼Ź¾æÉÖŖ£¬ŌŚ298KŹ±£¬µ±·“Ó¦“ļµ½Ę½ŗāŹ±c(N2O4)=0.6mol/L£¬ÓÉÓŚĘ½ŗāŹ±£¬N2O4µÄÅضČĪŖNO2µÄ2±¶£¬ŌņĘ½ŗāŹ±c(NO2)=0.3mol/L£¬ŌņøĆĪĀ¶ČĻĀµÄ»ÆŃ§Ę½ŗā³£ŹżK= c(N2O4)/ c2(NO2)= 0.6mol/L”Ā(0.3mol/L)2=6.67L/mol£»ÓÉÓŚ2NO2(g)![]() N2O4(g) ”÷H£½-akJ/mol(a>0)µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņĪüČȵÄÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌČō·“Ó¦ŌŚ398K½ųŠŠ£¬·“Ó¦“ļµ½Ę½ŗāŹ±µÄ»ÆŃ§Ę½ŗā³£ŹżK1<6.67”£Čō·“Ó¦ŌŚ398K½ųŠŠ£¬Ä³Ź±æĢ²āµĆn£ØNO2£©=0.3mol/L”¢n£ØN2O4£©=0.6mol/L£¬ŌņQ= c(N2O4)/ c2(NO2)= 0.6mol/L”Ā(0.3mol/L)2=6.67L/mol£¬ĖµĆ÷·“Ó¦Ī““¦ÓŚĘ½ŗāדĢ¬£¬·“Ó¦ÄęĻņ½ųŠŠ£¬Ņņ“Ėv£ØÕż£©<v£ØÄę£©£¬Ń”ĻīBÕżČ·”£
N2O4(g) ”÷H£½-akJ/mol(a>0)µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņĪüČȵÄÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌČō·“Ó¦ŌŚ398K½ųŠŠ£¬·“Ó¦“ļµ½Ę½ŗāŹ±µÄ»ÆŃ§Ę½ŗā³£ŹżK1<6.67”£Čō·“Ó¦ŌŚ398K½ųŠŠ£¬Ä³Ź±æĢ²āµĆn£ØNO2£©=0.3mol/L”¢n£ØN2O4£©=0.6mol/L£¬ŌņQ= c(N2O4)/ c2(NO2)= 0.6mol/L”Ā(0.3mol/L)2=6.67L/mol£¬ĖµĆ÷·“Ó¦Ī““¦ÓŚĘ½ŗāדĢ¬£¬·“Ó¦ÄęĻņ½ųŠŠ£¬Ņņ“Ėv£ØÕż£©<v£ØÄę£©£¬Ń”ĻīBÕżČ·”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)ij»ÆѧŠĖȤŠ”×éĄūÓĆĻĀĮŠŹŌ¼Į£ŗĢś·Ū”¢Šæ·Ū”¢0.1 mol”¤L1 FeCl3ČÜŅŗ”¢0.1 mol”¤L1 FeCl2ČÜŅŗ”¢KSCNČÜŅŗ”¢ŠĀÖĘĀČĖ®£¬Ģ½¾æFe2+”¢Fe3+µÄŃõ»ÆŠŌ”¢»¹ŌŠŌ£¬²¢ĄūÓĆŹµŃé½įĀŪ½ā¾öŅ»Š©ĪŹĢā”£
¢ŁÓĆĖłøųŹŌ¼ĮŠ“³öĢåĻÖFe2+¾ßÓŠ»¹ŌŠŌµÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_________________________________”£
¢ŚÉč¼ĘŹµŃé·½°ø£¬Ķź³ÉĻĀĮŠ±ķøń”£
Ģ½¾æÄŚČŻ | ŹµŃé·½°ø | ŹµŃéĻÖĻó |
Ģ½¾æFe3+¾ßÓŠŃõ»ÆŠŌ | ȔɣĮæ0.1 mol”¤L1 FeCl3ČÜŅŗ£¬ĶłČÜŅŗÖŠ¼ÓČė×ćĮæĢś·Ū£¬ŌŁ¼ÓČėÉŁĮæKSCNČÜŅŗ | ¼ÓČėĢś·Ūŗó£¬ČÜŅŗŃÕÉ«±äĪŖ________”£¼ÓČėKSCNČÜŅŗŗó£¬ČÜŅŗ________ |
¢ŪøĆŠĖȤŠ”×éĪŖĖµĆ÷”°Fe2+¾ßÓŠŃõ»ÆŠŌ”±£¬Ģį³öĮĖĻņFeCl2ČÜŅŗÖŠ¼ÓČėŠæ·Ū£¬¹Ū²ģŹµŃéĻÖĻóµÄ·½°ø£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_________________________________________”£
(2)ij·“Ó¦ÖŠ·“Ó¦ĪļÓėÉś³ÉĪļÓŠFe3+”¢Mn2+”¢H+”¢![]() ”¢H2OŗĶŅ»ÖÖĪ“ÖŖĄė×ÓX£¬ŅŃÖŖ
”¢H2OŗĶŅ»ÖÖĪ“ÖŖĄė×ÓX£¬ŅŃÖŖ![]() ŌŚ·“Ó¦ÖŠµĆµ½µē×Ó£¬ŌņXĄė×ÓŹĒ____________£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____________________________”£
ŌŚ·“Ó¦ÖŠµĆµ½µē×Ó£¬ŌņXĄė×ÓŹĒ____________£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____________________________”£
(3)ÓŠŅ»ĢśµÄŃõ»ÆĪļѳʷ£¬ÓĆ5 mol”¤L1µÄŃĪĖį140 mLĒ”ŗĆĶźČ«Čܽā£¬ĖłµĆČÜŅŗ»¹ÄÜÓėĶØČėµÄ0.56 LĀČĘų(±ź×¼×“æö)·“Ó¦£¬Ź¹Fe2+Č«²æ×Ŗ»ÆĪŖFe3+£¬Ōņ“ĖŃõ»ÆĪļĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¬ĪĀĶ¬Ń¹ĻĀ£¬µČÖŹĮæµÄO2ŗĶCO2Ļą±Č½Ļ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A.Ģå»ż±ČĪŖ8£ŗ11B.·Ö×ÓøöŹżÖ®±ČĪŖ11: 12
C.ĪļÖŹµÄĮæÖ®±ČĪŖ8£ŗ11D.Ō×ÓøöŹżÖ®±ČĪŖ11: 12
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ż³Ģ²»Éę¼°»Æѧ±ä»ÆµÄŹĒ
A. ŗ£Ė®Ģįäå B. ŹÆÓĶĮŃ»Æ C. ĆŗµÄĘų»Æ D. µāµÄÉż»Ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓĆ½šŹōÄĘŗĶæÕĘųÖʱø“æ¶Č½ĻøßµÄNa2O2£¬æÉĄūÓƵÄ×°ÖĆČēĻĀ”£»Ų“šĻĀĮŠĪŹĢā(×¢£ŗNa2O2æÉŅŌÓėH2O”¢CO2·“Ó¦)£ŗ
(1)×°ÖĆ¢ōÖŠŹ¢·ÅµÄŅ©Ę·ŹĒ________£¬Ęä×÷ÓĆŹĒ_______________________________”£
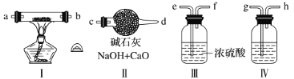
(2)Čō¹ę¶ØĘųĢåµÄĘųĮ÷·½Ļņ“Ó×óµ½ÓŅ£¬Ōņ×éŗĻŹµŃé×°ÖĆŹ±ø÷¼žŅĒĘ÷µÄÕżČ·Į¬½ÓĖ³ŠņĪŖ(°““Ó×óµ½ÓŅĖ³ŠņŠ“Ć÷ŅĒĘ÷µÄ±ąŗÅ¢ń”¢¢ņ””)____________£¬ø÷ŅĒĘ÷½ÓæŚµÄ±źŗÅ×ÖÄøĖ³ŠņŹĒ£ŗæÕĘų½ųČė________£¬________½Ó________£¬________½Ó________£¬________½Ó________(ÓĆ×ÖÄø±ķŹ¾)”£
(3)×°ÖĆ¢ņµÄ×÷ÓĆ_________________________________________”£
(4)²Ł×÷ÖŠĶØæÕĘųŗĶ¼ÓČȵÄĖ³ŠņĪŖ_______________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×éĄūÓĆČēĶ¼×°ÖĆ½ųŠŠ”°ĢśÓėĖ®·“Ó¦”±µÄŹµŃ飬²¢¼ģŃé²śĪļµÄŠŌÖŹ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

(1)A×°ÖƵÄ×÷ÓĆŹĒ__________________£¬BÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________________”£
(2)DµÄ×÷ÓĆŹĒ_______________________________________________”£
(3)EÖŠµÄĻÖĻóŹĒ____________________________________________________________”£
(4)A”¢BĮ½øö×°ÖĆÖŠÓ¦ĻȵćČ¼______“¦µÄ¾Ę¾«(Åē)µĘ£¬µćČ¼E“¦¾Ę¾«µĘÖ®Ē°Ó¦½ųŠŠµÄ²Ł×÷ŹĒ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°Ń1.1 gĢś”¢ĀĮ»ģŗĻĪļČÜÓŚ200 mL 5 mol”¤L£1ŃĪĖįÖŠ£¬·“Ó¦ŗóŃĪĖįµÄÅØ¶Č±äĪŖ4.6 mol”¤L£1(ČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę)”£Ēó£ŗ
(1)·“Ó¦ÖŠĻūŗÄHClµÄĪļÖŹµÄĮ棻
(2)øĆ»ģŗĻĪļÖŠĀĮ”¢ĢśµÄĪļÖŹµÄĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆŗĻĪļAŹĒŅ»ÖÖ²»ĪČ¶ØµÄĪļÖŹ£¬ĖüµÄ·Ö×Ó×é³ÉæÉÓĆOxFy±ķŹ¾£¬10mLAĘųĢåÄÜ·Ö½āÉś³É15mLO2ŗĶ10mLF2£ØĶ¬ĪĀĶ¬Ń¹ĻĀ£©”£
£Ø1£©AµÄ»ÆѧŹ½ŹĒ____________________________________________________________”£
£Ø2£©ŅŃÖŖA·Ö×ÓÖŠxøöŃõŌ×Ó³Ź”O”ŖO”ŖO”Į“דÅÅĮŠ£¬ŌņA·Ö×ӵĵē×ÓŹ½ŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŅĶ¼1ĪŖ¼×ĶéŗĶO2¹¹³ÉµÄČ¼ĮĻµē³ŲŹ¾ŅāĶ¼£¬µē½āÖŹČÜŅŗĪŖKOHČÜŅŗ£¬Ķ¼2ĪŖµē½āAlCl3ČÜŅŗµÄ×°ÖĆ£¬µē¼«²ÄĮĻ¾łĪŖŹÆÄ«”£ÓĆøĆ×°ÖĆ½ųŠŠŹµŃ飬·“Ó¦æŖŹ¼ŗó¹Ū²ģµ½xµē¼«ø½½ü³öĻÖ°×É«³Įµķ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
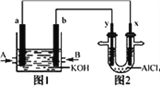
A. Ķ¼2ÖŠYµē¼«ĪŖŅõ¼«
B. Ķ¼2ÖŠ×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2AlCl3+6H2O2![]() 2Al(OH)3”ż+3Cl2”ü+3H2”ü
2Al(OH)3”ż+3Cl2”ü+3H2”ü
C. Ķ¼1ÖŠµē½āÖŹČÜŅŗµÄpHŌö“ó
D. Ķ¼1ÖŠµÄa µē¼«·“Ó¦Ź½ĪŖ£ŗCH4-8e-+8OH-=CO2+6H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com