
在下列反应中:A2(g)+B2(g)2AB(g) ΔH<0当其达到平衡时,在下图所示的曲线中,符合勒夏特列原理的是( )
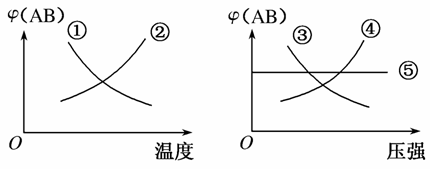
A.①② B.③④
C.① D.①⑤
科目:高中化学 来源: 题型:
日常所用干电池的电极分别为碳棒(上面有铜帽)和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2吸收H2),电极反应式可简化为:
Zn-2e-—→Zn2+,2NH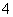 +2e-—→2NH3↑+H2↑(NH3与Zn2+能生成一种稳定的物质)。根据上述判断,下列结论不正确的是( )
+2e-—→2NH3↑+H2↑(NH3与Zn2+能生成一种稳定的物质)。根据上述判断,下列结论不正确的是( )
A.Zn为正极,碳为负极
B.Zn为负极,碳为正极
C.工作时,电子由Zn极经过导线流向碳极
D.长时间连续使用时,内装糊状物可能流出腐蚀用电器
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
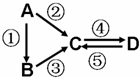
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:______________________________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:__________________。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:__________________________________。
(4)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式:__________________________。
(5)若A为淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质. B与C可反应生成A。请写出B的电子式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
.水溶液X中只可能溶有K+、Mg2+、Al3+、AlO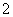 、SiO
、SiO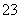 、SO
、SO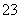 、CO
、CO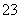 、SO
、SO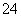 中的若干种离子。某同学对该溶液进行了如图实验:
中的若干种离子。某同学对该溶液进行了如图实验:
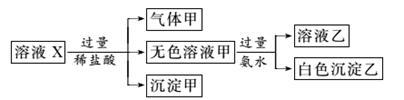
下列判断正确的是( )
A.气体甲一定是纯净物
B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、AlO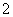 和SiO
和SiO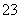 一定存在于溶液X中
一定存在于溶液X中
D.CO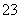 和SO
和SO 一定不存在于溶液X中
一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用化学平衡移动原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
B.加催化剂,使N2和H2在一定条件下转化为NH3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,将1mol的CO和水蒸气通入容器中发生下述反应:CO(g)+H2O(g)CO2(g)+H2(g),达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,又达到平衡后,CO2的物质的量是( )
A.等于0.6mol
B.等于1mol
C.大于0.6mol小于1mol
D.大于1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中充入3mol气体A和2.5mol气体B,发生反应:3A(g)+B(g)xC(g)+2D(g)(正反应为吸热反应),5min时测得生成1mol D,C的平均反应速率v(C)=0.1mol·L-1·min-1,试求:
(1)方程式中C的化学计量数x=__________。
(2)5min内A的平均反应速率v(A)=__________。
(3)5min时B的转化率为__________。
(4)温度升高A的转化率________(填“增大”或“减小”或“不变”下同),压强增大B的转化率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中四条曲线分别表示ⅣA、ⅤA、ⅥA、ⅦA族元素的气态氢化物的沸点,a、b、c分别为三种氢化物,
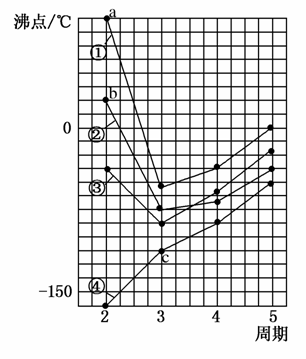
(1)其中表示ⅥA元素气态氢化物沸点的是曲线________(填标号,下一空同),表示ⅣA族元素气态氢化物沸点的是曲线________。
(2)a的电子式为________,b的空间构型为________,c的化学式为________。
(3)同一族中第3、4、5周期元素的气态氢化物沸点依次升高,其原因是________________。曲线中第2周期元素的气态氢化物的沸点显著高于第3周期元素气态氢化物的沸点,其原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素周期表的说法中,错误的是()
A. 元素周期表是元素按原子序数大小排列而成的
B. 元素原子的电子层数等于其所在周期的周期序数
C. L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D. 元素周期表是元素周期律的具体表现形式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com