
【题目】下列叙述正确的是
A. 1.00mol NaCl中含有6.02×1023个NaCl分子
B. 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C. 欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D. 电解58.5g熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。设起始
CO(g)+3H2(g)。设起始![]() =Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法正确的是
=Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法正确的是

A.该反应的焓变 △H>0
B.图中Z的大小为 a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后φ(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验:
① 用蓝色石蕊试纸检测该溶液,试纸显红色;
② 取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色
③ 取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④ 取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤ 取实验 ④ 后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。 请回答下列问题:
(1)根据上述实验判断原溶液中肯定存在的离子是______________,肯定不存在的离子是__________。
(2)写出实验②的离子方程式:______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液(混合液)的pH如下表,请回答:
实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | C | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,仅从甲组情况分析,如何用a (混合液的pH)来说明HA是强酸还是弱酸__________。
(2) 不考虑其它组的实验结果,仅从乙组情况分析,C是否一定等于0.2__________(填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________。
(3)丙组实验结果分析,HA是__________酸(填“强”或“弱”)。该组混合液中离子浓度由大到小的顺序是__________。
(4)丁组实验混合液中由水电离出的c(OH-)=__________molL﹣1,写出该混合液中下列算式的精确结果(不需做近似计算)。
c(Na+)-c(A-)=__________molL-1, c(OH-)-c(HA)=__________molL-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
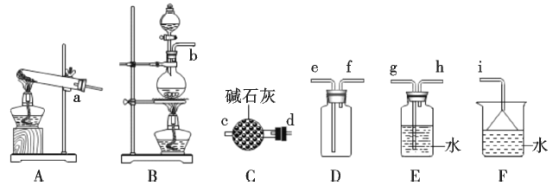
(1)氨气的制备
①氨气的发生装置中反应的化学方程式为__。装置C的仪器名称__。
②欲收集一瓶干燥的氨气,选择上图中的装置,其接口连接顺序为a→__(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
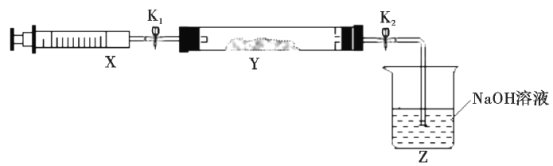
操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中__ | ②反应的化学方程式___ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
打开K2 | ③__ | ④___ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Mg—Cu合金11.2g完全溶解于硝酸中,反应产生的X气体,再向所得溶液中加入NaOH溶液,恰好完全反应时产生21.4g沉淀,根据题意推断X气体的成份可能是
A. 0.3molNO
B. 0.2molNO2和0.1molN2O4
C. 0.1molNO、0.2molNO2和0.05molN2O4
D. 0.1molNO、0.1molNO2和0.2molN2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验现象的预测正确的是( )
A.  振荡后静置,溶液不再分层,且保持无色透明
振荡后静置,溶液不再分层,且保持无色透明
B.  铁片最终完全溶解,且高锰酸钾溶液变无色
铁片最终完全溶解,且高锰酸钾溶液变无色
C.  微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终无明显变化
微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终无明显变化
D.  当液体变成红褐色时,停止加热,让光束通过分散系时可产生丁达尔效应
当液体变成红褐色时,停止加热,让光束通过分散系时可产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(假设还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol·L-1NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。

(1)生成的NO在标况下的体积为___________L。
(2)Cu的物质的量为_________mol。
(3)稀硝酸的浓度为___________mol/L。
(4)a的值为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图。
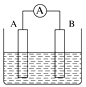
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是__(填字母)。
A 铝片、铜片 B 铜片、铝片
C 铝片、铝片 D 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:____。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:___;该电池在工作时,A电极的质量将_(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:_________;该电池在工作一段时间后,溶液的碱性将___(填“增强”“减弱”或“不变”)。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:________;若该电池反应消耗了6.4克CH4,则转移电子的数目为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com