
(15分)溴化钙在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
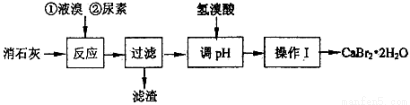
溴化钙的部分溶解度数值如下:
温度 | 0℃ | 10℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
溶解度(g) | 125 | 132 | 143 | 213 | 278 | 295 | 312 |
(1)6Ca(OH)2+6Br2 50~70℃ 5CaBr2+6H2O+Ca(BrO3)2,每生成1 mol Ca(BrO3)2转移电子的物质的量为 ;50~70℃时,尿素[CO(NH2)2]将生成的Ca(BrO3)2还原为CaBr2,尿素被氧化为N2,该反应的化学方程式为 。
(2)过滤所需的玻璃仪器有玻璃棒、,。
(3)加入氢溴酸调pH的作用是。
(4)操作I包括、、过滤、、干燥。
(5)“二氧化硫法”制备的氢溴酸粗品中常含有少量的溴和硫酸;请选用所提供的试剂,补充完整检验氢溴酸粗品中是否含有Br2相SO42-的实验方案。
限选下列试剂:氯水、淀粉KI溶液、CCl4、BaCl2溶液、稀盐酸、植物油。
(1)10moL;2CO(NH3)2+Ca(BrO3)2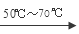 CaBr2+2CO2↑+2N2↑+4H2O;
CaBr2+2CO2↑+2N2↑+4H2O;
(2)烧杯、漏斗;(3)除去过量的氢氧化钙;(4)蒸发浓缩、冷却结晶、冰水洗涤(或乙醇洗涤);
(5)①取少量的氢溴酸粗产生与试管中,滴加少量植物油,将长滴管插入液面下滴加淀粉KI溶液变为蓝色,说明含有Br2;否则不含有Br2。②另取少量氢溴酸粗产品与试管中,滴加少量稀盐酸,再加入BaCl2溶液,若产生白色沉淀,说明含有SO42-;否则不含SO42-。
【解析】
试题分析:(1)根据氧化还原反应中元素化合价升降的数目等于反应过程中的电子转移数目可知:每生成1 mol Ca(BrO3)2转移电子的物质的量为10mol;在50~70℃时,尿素[CO(NH2)2]与Ca(BrO3)2反应产生CaBr2和N2,该反应的化学方程式为2CO(NH3)2+Ca(BrO3)2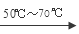 CaBr2+2CO2↑+2N2↑+4H2O;(2)过滤所需的玻璃仪器有玻璃棒、漏斗、烧杯;(3)加入氢溴酸调pH的作用是除去过量的氢氧化钙,以形成CaBr2·2H2O;(4)从溴化钙的溶液中分离得到晶体的操作I包括蒸发浓缩、冷却结晶、冰水洗涤(或乙醇洗涤)、干燥。(5)“二氧化硫法”制备的氢溴酸粗品中常含有少量的溴和硫酸;检验氢溴酸粗品中是否含有Br2相SO42-的实验方案是①取少量的氢溴酸粗产生与试管中,滴加少量植物油,将长滴管插入液面下滴加淀粉KI溶液变为蓝色,说明含有Br2;否则不含有Br2。②另取少量氢溴酸粗产品与试管中,滴加少量稀盐酸,再加入BaCl2溶液,若产生白色沉淀,说明含有SO42-;否则不含SO42-。
CaBr2+2CO2↑+2N2↑+4H2O;(2)过滤所需的玻璃仪器有玻璃棒、漏斗、烧杯;(3)加入氢溴酸调pH的作用是除去过量的氢氧化钙,以形成CaBr2·2H2O;(4)从溴化钙的溶液中分离得到晶体的操作I包括蒸发浓缩、冷却结晶、冰水洗涤(或乙醇洗涤)、干燥。(5)“二氧化硫法”制备的氢溴酸粗品中常含有少量的溴和硫酸;检验氢溴酸粗品中是否含有Br2相SO42-的实验方案是①取少量的氢溴酸粗产生与试管中,滴加少量植物油,将长滴管插入液面下滴加淀粉KI溶液变为蓝色,说明含有Br2;否则不含有Br2。②另取少量氢溴酸粗产品与试管中,滴加少量稀盐酸,再加入BaCl2溶液,若产生白色沉淀,说明含有SO42-;否则不含SO42-。
考点:考查氧化还原反应中的电子转移、混合物的分离操作方法、化学方程式的书写、Br2、SO42-的检验方法的知识。


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
下列有关工业生产的叙述正确的是
A.合成氨工业中,将NH3及时液化分离有利于加快反应速率
B.氯碱工业中,使用离子交换膜可防止C12和NaOH溶液反应
C.硫酸工业中,接触室内安装热交换器,是为了利用沸腾炉中排出的SO2的热量
D.硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:选择题
下列与含氯化合物有关的说法正确的是
A.HClO是弱酸,所以NaClO是弱电解质
B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
D.电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:选择题
近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂。高铁酸钾在水处理过程中涉及到的过程正确的有:
①蛋白质的变性 ②蛋白质的盐析 ③胶体的聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
A.①②③④ B.①③④⑥ C.②③④⑤ D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:选择题
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是
A.使酚酞变红色的溶液:Na+、Ba2+、I-、Cl-
B.使甲基橙变红色的溶液:Fe2+、K+、NO3-、SO42-
C.含有0.1 mol·L-1 Fe3+的溶液:Na+、K+、SCN-、NO
D.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg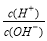 ,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )
,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )

A.A点时加入氢氧化钠溶液体积为20 mL
B.室温时0.01 mol·L-1的醋酸溶液pH=4
C.OA段溶液中:c(CH3COO-)> c(CH3COOH)
D.若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH) = c(OH-) - c(H+)
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.氯化铝溶液中加入过量的氨水:Al3++4 NH3·H2O=AlO2-+4 NH4+
B.稀硝酸中加入过量铁粉:Fe+4H++NO3- = Fe3++NO↑+2H2O
C.二氧化锰与浓盐酸混合加热:MnO2+4H++2Cl- △ Mn2++ Cl2↑+2H2O
D.石灰水中加入过量小苏打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2015届广西桂林市高三上学期第一次月考化学试卷(解析版) 题型:选择题
某反应体系中存在下列六种物质:As2S3、HNO3、H2SO4、NO、H3AsO4和H2O,已知其中As2S3是反应物之一。下列说法不正确的是
A、该反应属于氧化还原反应
B、此反应中只有砷元素被氧化,只有氮元素被还原
C、HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物
D、HNO3、H2SO4、H3AsO4都是最高价氧化物对应的水化物
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三8月月考化学试卷(解析版) 题型:选择题
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
| 操作 | 现象 | 结论 |
A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com