
| X | ||
| Y | Z |
| A. | 氧、磷、氯 | B. | 氮、硅、硫 | C. | 氟、硫、氩 | D. | 碳、铝、磷 |
分析 X、Y、Z 均为短周期元素,所以它们应周期表的1、2、3周期,由于X 所在族位于Y 和Z 的中间,所以X、Y、Z 只能是第2和第3周期的元素,设X 的原子序数为x,则根据Y 和Z 与X 的相对位置关系可知,Y 的原子序数为x+7,Z 的原子序数为x+9,再根据Y、Z 两元素原子序数之和为X 元素原子序数的4倍,则可求得x=8,X、Y、Z 依次为氧、磷、氯,由此分析解答.
解答 解:X、Y、Z 均为短周期元素,所以它们应周期表的1、2、3周期,由于X 所在族位于Y 和Z 的中间,所以X、Y、Z 只能是第2和第3周期的元素,设X 的原子序数为x,则根据Y 和Z 与X 的相对位置关系可知,Y 的原子序数为x+7,Z 的原子序数为x+9,再根据Y、Z 两元素原子序数之和为X 元素原子序数的4倍,则可求得x=8,X、Y、Z 依次为氧、磷、氯,
故选A.
点评 本题是考查学生对元素周期表和原子序数之间的关系的掌握情况,要求学生熟悉周期表的结构,熟记1到20号元素在周期表的位置.根据元素在周期表的位置特点,确定元素的种类,是对元素周期表中的“位”“构”“性”三者关系的简单综合应用.当然本题目也可以用排除法来解决.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等.运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等.
2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等.运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
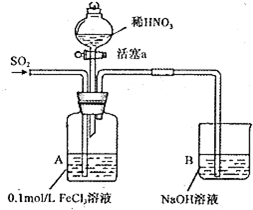
| 实验 序号 | 实验操作 | 实验现象 |
| I | 向A装置中通入一段时间的SO2气体. | A中黄色溶液最终变为浅绿色. |
| II | 取出少量A装置中的溶液,先加入 KSCN溶液,再加入BaCl2溶液. | 加人KSCN溶液后溶液不变色;再加入BaCl2溶液产生白色沉淀. |
| III | 打开活塞a,将过量稀HNO3加入装置A 中,关闭活塞a. | A中浅绿色溶液最终变为黄色. |
| V | 取出少量A装置中的溶液,加入KSCN 溶液. | 溶液变为红色. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 加入盐酸 | 产生无色气体 | 溶液中一定含有CO32- |
| B | 加入KSCN溶液 | 显血红色 | 溶液中一定含有Fe3+ |
| C | 加入盐酸酸化的氯化钡溶液 | 生成白色沉淀 | 溶液中一定含有SO42- |
| D | 取未知溶液进行焰色反应 | 火焰显黄色 | 溶液中一定含有K+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO | B. | NH3 | C. | CO2 | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
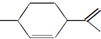 .下列关于它的说法不正确的是( )
.下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | |
| B. | 1mol该有机物能与4mol H2发生加成反应 | |
| C. | 能与溴水发生加成反应 | |
| D. | 常温下呈液态,难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com