
科目:高中化学 来源: 题型:阅读理解
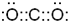
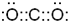
| ||
| ||

| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
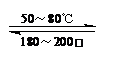 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H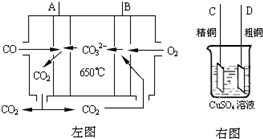
| 10 |
| 11 |
| ||
| 氢离子 |
| 石灰水 |
查看答案和解析>>
科目:高中化学 来源:广东省2009届高三化学各地名校月考试题汇编-有机推断(2) 题型:022
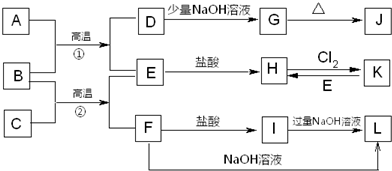
请根据下图作答:
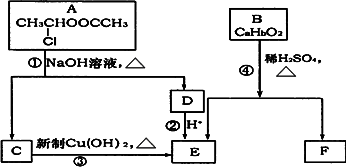
已知:一个碳原子上连有两个羟基时,易发生下列转化:
(1)E中含有的官能团是________.
(2)反应③的化学方________.
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2)∶n(H2O)=2∶1,则B的分子式为________.
(4)F是高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种.F在一定条件下发生加聚反应的化学方程式为________.
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应.G有多种结构,写出其中一种的结构简式_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
2009年12月18日凤凰网报道,经过北京顶级中西医专家长达7个月的科研攻关,终于制出一种有效治疗甲型H1N1流感的新中药“金花清感方”。其主要成分之一是金银花,而金银花的有效成分之一是绿原酸。下面是有关绿原酸的分子结构及其转化关系,其中E为芳香烃,其苯环上的一氯代物只有一种(部分产物省略)

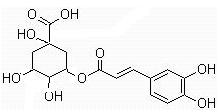
请回答下列问题:
(1)绿原酸的分子式是 ;A中含氧官能团的名称为 ;H的结构简式为 。
(2)①的反应类型是 ;1mol绿原酸最多消耗 molNaOH。
(3)芳香烃E的同分异构体(与E含有相同的取代基)的沸点由大到小的顺序是(包括E在内) (用结构简式表示)。
(4)写出反应③、④的化学方程式:
③ ;
④ 。
(5)B是咖啡酸,它有多种同分异构体,写出满足下列条件的所有同分异构体的结构简式:(条件:a.苯环上含有两个取代基,且苯环上的一氯代物只有两种;b.能发生水解反应,且产物之一能发生银镜反应;c.能与碳酸氢钠溶液反应) 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库。目前,世界各国都在研究如何充分利用海洋资源。
(1)全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg·L-1。其工业提取法有:
Ⅰ、空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴。该方法涉及的反应有:
①_________________(写出离子方程式);
②3Br2+3CO32-=BrO3-+5Br-+3CO2↑;
③_________________(写出离子方程式)。
其中反应②中氧化剂是_________,还原剂是___________
Ⅱ、空气吹出SO2吸收法。该方法基本同⑴,只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴。
写出溴与二氧化硫反应的化学方程式 ____________________ 。
Ⅲ、溶剂萃取法。该法是利用单质溴在水中和萃取剂中溶解度的不同的原理来进行的。
实验室中萃取用到的实验仪器名称是 ___________________。
下列可以用于海水中溴的萃取的试剂是 __________。①乙醇,②四氯化碳,③硝酸
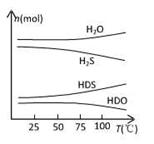 (2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。
(2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。
右图为“硫化氢-水双温交换法”所发生的两个
反应中涉及的四种物质在反应体系中的物质的量随温
度的变化曲线。写出100℃时所发生的反应的化学方
程式________________________________________;
工业上富集HDO的生产过程中,可以循环利用的一种
物质是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com