
【题目】14g Cu、Ag合金与足量某浓度的硝酸反应,将放出的气体与1.12L O2(标况)混合,恰好能被水全部吸收生成硝酸,则合金中Cu的质量为( )
A.1.6g
B.3.2g
C.6.4g
D.9.6g
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4![]() Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
(1)取少量分解得到的固体加入稀盐酸溶解,为检验溶液中是否有Fe3+,下列试剂或药品中最合适的是 (填序号),加入该试剂后可观察的现象为 。
A.稀盐酸 B.氯气 C.KSCN溶液 D.氯化铜溶液
(2)将高温分解产生的气体通入下图所示装置中,以检验产生的气体成分。
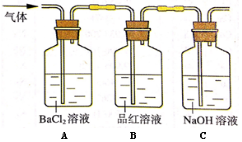
请回答下列问题:
①若在装置A中,观察到有白色沉淀生成,则该沉淀为 ,表明有 气体存在。
②装置C中的NaOH溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为从海带中提取碘的工业生产过程,有关说法错误的是
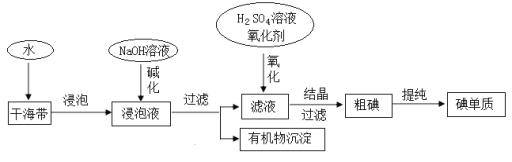
A.因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘元素
B.碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀
C.在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等
D.在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预测,氨有望取代氢能,成为重要的新一代绿色能源.下列有关说法不正确的是( )
A.液氨作为清洁能源的反应原理是4NH3+5O2 ![]() 4NO+6H2O
4NO+6H2O
B.液氨具有腐蚀性和毒性,在使用过程中要防止液氨泄漏
C.氨气比空气轻,标准状况下密度约为0.76 g?L﹣1
D.氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJmol﹣1)P﹣P:198 P﹣O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( ) 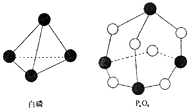
A.释放1638kJ的能量
B.吸收1638kJ的能量
C.释放126kJ的能量
D.吸收126kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性强弱:Br<Fe2+。往100ml溴化亚铁溶液中缓慢通入2.24 L(标准状况)氯气,反应完成后溶液中有1/2的Br被氧化成Br2。则原溴化亚铁溶液的物质的量浓度为
A. 1.0mol/L B. 1.5mol/L C. 1.1mol/L D. 1.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)2AB(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( ) 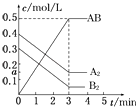
A.图中a点的值为0.15
B.该反应的平衡常数K=0.03
C.温度升高,平衡常数K值减小
D.平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2A(g)B(g)+D(g)在密闭容器中分别在下列四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(molL﹣1)随反应时间(min)的变化情况如下表:
时间 | 1 | 10 | 20 | 30 | 40 | 50 | 60 | |
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)实验1中,在10~20min时间内,以A的速率表示的平均反应速率为molL﹣1min﹣1
(2)实验2中,A的初始浓度c2=molL﹣1 , 反应经20min就达到平衡,可推测实验2中还隐含的条件是 .
(3)设实验3的化学反应速率为v3 , 实验1的化学反应速率为v1 , 则v3v1(填“>”“=”或“<”),且c31.0molL﹣1(填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应的正反应是反应(填“吸热”或“放热”),理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com