
【题目】类比法是化学学习过程中一种重要方法,以下类比关系正确的是( )
A.工业上可以电解熔融的氯化镁或氯化铝制得相应的金属单质
B.Cl2、Br2、I2都具有强氧化性,都能将铁氧化成+3价的铁盐
C.二氧化碳和二氧化硫都是氧化物,两者都不能和氯化钙溶液反应
D.氧化铁和氧化亚铁都是碱性氧化物,和硝酸反应都只生成盐和水
科目:高中化学 来源: 题型:
【题目】化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6。分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198 P—O:360 O===O:498

若生成1 mol P4O6,则反应P4(白磷)+3O2===P4O6中的能量变化为
A.吸收1 638 kJ能量
B.放出126 kJ能量
C.吸收126 kJ能量
D.放出1 638 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物。请回答下列问题:
(1)写出元素E在周期表中的位置: ;判断物质X中存在的化学键类型 。
(2)C、D、E分别形成的简单离子半径由大到小的顺序是: (用离子符号表示);C、E氢化物的热稳定性比较 (用具体物质化学式比较)。
(3)B元素的氢化物可以在实验室中制取,

①写出B元素氢化物的电子式 ,其实验室发生装置可以选择上图中的_________,常用的实验室制备反应的化学方程式为___________ ____。
②欲制备并收集一瓶干燥的该气体,选择上图中的装置,其连接顺序为:(按气流方向,用导管口字母表示)____ __。
③欲证明上述盐X溶液中含有的阳离子,其方法是 。
(4)E的最高价态与A、B、C三种元素形成的酸式盐Y在水溶液中的电离方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Cr2O3样品中含有少量Al2O3、MgO等杂质。实验室以此样品为主要原料制取重铬酸钾(K2Cr2O7)的流程如下:
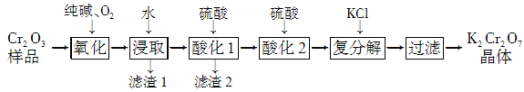
已知:2CrO42-+2H+![]() Cr2O72-+H2O。
Cr2O72-+H2O。
(1) 上述氧化过程中,若将1 mol Cr2O3转化成Na2CrO4,消耗氧气的体积(标准状况)是________。
(2) 酸化1中为确保溶液中Al3+、AlO2-浓度均不超过10-6 mol·L-1,需调节溶液pH的范围是________。
已知:Al(OH)3(s) ![]() H++AlO2-+H2O的K=1×10-14;Ksp[Al(OH)3]=1×10-33
H++AlO2-+H2O的K=1×10-14;Ksp[Al(OH)3]=1×10-33
(3)酸化2后所得溶液加入KCl发生复分解反应,该反应能发生的原因是_________________。
(4) 称取重铬酸钾试样2.40 g 配成250 mL溶液,取出25.00 mL于碘量瓶中,加入稀硫酸和足量碘化钾(铬被还原为Cr3+)并放于暗处6min左右,然后加入适量水和数滴淀粉指示剂,用0.24 mol·L-1 Na2S2O3标准溶液滴定至终点(发生反应:I2+2S2O32-===2I-+S4O62-,杂质不参与反应),共用去Na2S2O3标准溶液20.00mL。求所得产品中重铬酸钾的质量分数(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )

A. 原子半径Z<M
B. Y的最高价氧化物对应水化物的酸性比X的弱
C. X的最简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第2周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学反应方程式
(1)在25℃, 101kPa下, 23g乙醇完全燃烧生成CO2和液态水时放热321.4kJ。则表示乙醇燃烧热的热化学方程式为_____________;
(2)室温下,稀H2SO4和稀KOH溶液发生中和反应,对应的中和热的热离子方程式为_____________;
(3)在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5mol电子转移时,放出650 kJ的热量,则表示该反应的热化学方程式为(要求C2H2的系数为1) _____________;
(4) 在25℃, 101kPa下,已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则2mol NH3完全分解生成N2与H2时,对应的热化学方程式为_____________;
(5) 己知:C(石墨)+O2(g)═CO2(g)△H1=-393.5kJ/mol
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ/mol
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599.2kJ/mol,
计算25℃时,由C(石墨)和H2(g)反应生成1molC2H2(g)的△H= _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表一部分,列出了十个元素在周期表中的位置:
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | |||||||
3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
4 | ② | ④ | ⑨ |
请用化学用语回答下列问题
(1)在①~⑦元素中,原子半径最大的是 (填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是 (填物质化学式),⑤所对应元素的单质工业制备方法为 。
(3)用电子式表示元素③与⑧形成化合物的过程 。
(4)我国首创以单质⑤—空气—海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使单质⑤不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极反应是 ,正极反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)===2H2O(l) ΔH1=-571.8 kJ·mol-1
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH2=-192.9 kJ·mol-1
(1)甲醇蒸气完全燃烧的热化学方程式为______________________________
(2)反应②中的能量变化如图所示,该反应为 (吸或放)热反应,ΔH2=________。(用E1、E2表示)
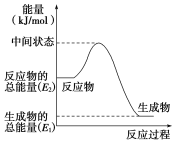
(3)H2(g)的燃烧热为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下列七种有机物中:①CH4 ②CH2=CH2 ③![]() ④CH3COOH ⑤HOCH2CHO ⑥CH3CH2CH2CH3 ⑦葡萄糖 ⑧蛋白质 ⑨淀粉
④CH3COOH ⑤HOCH2CHO ⑥CH3CH2CH2CH3 ⑦葡萄糖 ⑧蛋白质 ⑨淀粉
(1)可与浓硝酸发生颜色反应的是______________(填序号,下同)。
(2)属于同系物的是__________
(3)互为同分异构体的是___________。.
(4)易发生银镜反应的是______________
II.在5L的密闭容器中充入1mol A 和2mol B,在一定条件下发生反应4A(g)+5B(g)![]() 4C(g)+6D(g),半分钟后,C的物质的量增加了0.30mol.
4C(g)+6D(g),半分钟后,C的物质的量增加了0.30mol.
(5)D的平均反应速率为 .
(6)A的转化率为
(7) 不能判断该反应已达平衡状态的是
A 单位时间内生成n mol A的同时生成2n mol D的状态
B 生成物浓度不再变化的状态 .
C 混合气体的平均相对分子质量不再改变的状态.
D 混合气体的压强不再改变的状态
E 容器中各组分的体积分数不随时间变化的状态
F 容器中A、B、C、D的物质的量的比一定是4:5:4:6的状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com