
实验桌上只有烧碱、盐酸、铜片、大理石、蒸馏水五种试剂,从欠缺试剂的角度来看(实验仪器齐全),无法进行的实验项目是
A.制取氢气 B.制取碳酸钠
C.制取氯化铜 D.测定盐酸的浓度
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源:2014高考名师推荐化学化学平衡图像的分析(解析版) 题型:填空题
已知CO2(g)+3H2(g)  CH3OH(l)+H2O(l) ΔH=-130.9 kJ·mol-1
CH3OH(l)+H2O(l) ΔH=-130.9 kJ·mol-1
(1)现将0.8 mol CO2和2.4 mol H2 充入容积为20 L的密闭容器中发生上述反应,下列说法正确的是__________(填字母序号)。
A.该反应在低温下能自发进行
B.当容器内CO2气体体积分数恒定时,该反应已达平衡状态
C.若其他条件不变,实验测得平衡常数:K(T1)>K(T2),则T1<T2
D.现有该反应的X、Y两种催化剂,X能使正反应速率加快约5×105倍、Y能使逆反应速率加快约8×106倍(其他条件相同),故在生产中应该选择X为催化剂更合适
(2)该反应进行到45 s时达到平衡,此时CO2的转化率为68.75%。下图1中的曲线表示该反应在前25 s内的反应进程中CO2浓度变化。
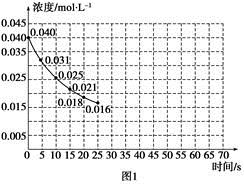
①若反应延续至70 s。请在图1中用实线画出25 s至70 s的反应进程曲线。
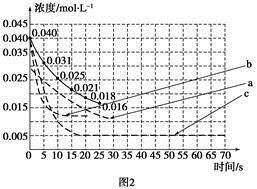
②某化学兴趣小组采用实验对比法分析改变实验条件对该反应进程的影响,每次只改变一个条件,并采集反应进程中CO2的浓度变化,在原有反应进程图像上绘制对应的曲线。实验数据如下表:
实验 编号 | CO2起始 浓度/mol·L-1 | 反应温 度/℃ | 反应压 强/kPa | 是否加入 催化剂 |
A | 0.030 | 150 | 101 | 否 |
B | 0.040 | 150 | 101 | 否 |
C | 0.040 | 250 | 101 | 是 |
但是该小组负责绘制图线的学生未将曲线(虚线)绘制完整(见图2),也忘记了注明每条曲线所对应改变的条件,请把每个实验编号与图2中对应曲线的字母进行连线。
实验编号 图2中字母
A a
B b
C c
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学反应速率的计算、影响因素(解析版) 题型:选择题
在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(g)。2 min末该反应达到平衡,生成 0.8 mol D,并测得C的浓度为0.2 mol·L-1,下列判断正确的是
xC(g)+2D(g)。2 min末该反应达到平衡,生成 0.8 mol D,并测得C的浓度为0.2 mol·L-1,下列判断正确的是
A.平衡常数约为0.3
B.B的转化率为60%
C.A的平均反应速率为0.3 mol/(L·min)
D.若混合气体的密度不变则表明该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学反应中能量变化的有关概念及计算(解析版) 题型:选择题
下列关于反应热和热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3) kJ·mol-1
B.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ·mol-1
C.氢气的燃烧热为285.5 kJ·mol-1,则电解水的热化学方程式为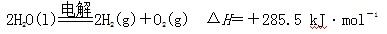
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学制备实验方案的设计与评价(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源,对今后世界经济发展有着决定性作用。下列有关说法正确的是

A.整个过程可在实验室中模拟进行
B.工段②是风化过程
C.在工段③④⑤中溴元素均被氧化
D.工段①中除去粗盐中的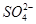 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学元素周期表及其应用(解析版) 题型:选择题
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。已知Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
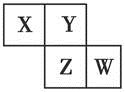
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.氢化物的稳定性:X>Y>Z
D.四种元素的单质中,Z单质的熔、沸点最高
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学元素周期律及其应用(解析版) 题型:选择题
目前人类已发现的非金属元素除稀有气体外共有16种,对这16种非金属元素的相关判断( )
①都是主族元素,最外层电子数都大于4
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以又叫作气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤根据非金属原子最外层的电子数,可判断两种元素得电子能力的强弱
⑥非金属得电子后形成的简单阴离子的核外电子排布一定与上一周期稀有气体原子的核外电子排布相同
A.④⑤正确 B.①③⑥正确
C.②③⑤正确 D.都错误
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学STS应用(解析版) 题型:选择题
化学知识在生产和生活中有着重要的应用。下列说法中,错误的是
A.与铜质水龙头连接处的钢质水管易发生腐蚀
B.明矾常作为净水剂,双氧水通常可用于作杀菌消毒
C.食物中可加入适量的食品添加剂,如香肠中可以加少量的亚硝酸钠以保持肉质新鲜
D.金属钠、镁等活泼金属着火时,可以使用泡沫灭火器灭火
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com