
下表为有关化合物的pKsp,pKsp=-lgKsp。某同学设计实验如下:①向AgNO3溶液中加入适量N aX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY;③向②中加入Na2Z,沉淀又转化为Ag2Z。则表中a、b、c的大小关系为( )
aX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY;③向②中加入Na2Z,沉淀又转化为Ag2Z。则表中a、b、c的大小关系为( )
| 相关化合物 | AgX | AgY | Ag2Z |
| pKsp | a | b | c |
A.a>b>c B.a<b<c
C.c<a<b D.a+b=c
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
用一种只有水分子能自由通过而直径较大的溶质分子不能通过的隔膜把水槽隔离成大小完全相同的甲、乙两室,甲室中装入淀粉溶液,乙室中装入蒸馏水(如图)。此时甲、乙两室中的水分子均可自由地通过隔膜而相互扩散,已知这种扩散速度与单位体积内溶质的微粒数成反比,而与液体的压强成正比。
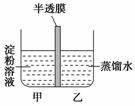
根据以上叙述回答下列问题:
(1)若甲、乙两室中装入液体的体积相同,对于实验开始阶段的描述正确的是________。
A.水分子从甲室向乙室的扩散速度大于乙室向甲室的扩散速度
B.水分子从乙室向甲室的扩散速度大于甲室向乙室的扩散速度
C.两室中水分子的相互扩散速度相等
D.两室中水分子的扩散速度将越来越小
(2)相同温度下,甲室装入质量分数为1%的尿素[CO(NH2)2]水溶液,乙室装入等体积的质量分数为a%的葡萄糖(C6H12O6)溶液,若两溶液的密度近似看成1 g·cm-3,且水分子相互扩散的速度也相等,则a的近似值是________。
A.1 B.2
C.3 D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
芳香族化合物A、B、C的分子式均为C8H8O2,苯环上只有一个侧链,其性质如下:
| 物质 性质 | 与NaOH溶液 | 与银氨溶液 | 与钠 |
| A | 水解 | 不产生银镜 | 不反应 |
| B | 中和 | 不产生银镜 | 产生H2 |
| C | 水解 | 产生银镜 | 不反应 |
写出A、B、C的结构简式:
A 或 ;B C
查看答案和解析>>
科目:高中化学 来源: 题型:
以下进行性质比较的实验设计,不合理的是
A.比较镁、铝金属性:镁、铝(除氧化膜)分别放入4 mol·L-1NaOH溶液中
B.比较氯、溴非金属性:氯气通入溴化钠溶液中
C.比较Cu、Fe2+的还原性:Cu加入FeCl3溶液中
D.比较高锰酸钾、氯气的氧化性:高锰酸钾中加入浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
达州市渠县境内含有丰富的深层地下食盐资源,食盐是日常生活中的必需品,也是重要的化工原料。
(1)经测定该县深层地下粗盐中含有少量K+、Ca2+、Mg2+、Fe3+等杂质离子,某研究性学习小组在实验室提纯NaCl的流程如下:
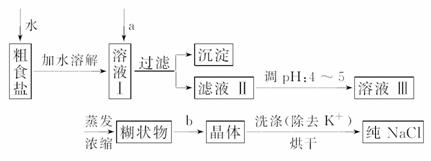
所提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇溶液、CCl4,仪器及用品自选。
①欲除去溶液中的Ca2+、Mg2+、Fe3+、SO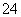 ,选出a操作中所代表的试剂,按滴加顺序依次为_________________________________________________________(只填化学式),
,选出a操作中所代表的试剂,按滴加顺序依次为_________________________________________________________(只填化学式),
b步操作的名称是____________。
②洗涤除去NaCl晶体表面附带的少量KCl,应选用试剂是____________,用pH试纸测定滤液ⅡpH值的方法是______________________________________________。
(2)用提纯的NaCl配制500 mL,2.5 mol·L-1的NaCl溶液,所需仪器除烧杯,托盘天平(砝码和镊子),药匙,玻璃棒外,还需要____________________________________(填仪器名称),应称取NaCl________ g。
(3)下列操作会导致所配NaCl溶液浓度偏高的是___________________________。
A.定容完毕后,盖塞,摇匀,再将容量瓶置于实验台上,发现液面低于刻度线,再添加蒸馏水至刻度线
B.未将洗涤烧杯内壁的溶液转入容量瓶
C.定容时,俯视刻度线
D.转移溶液之前,容量瓶内有少量蒸馏水
E.称量时,天平指针指向左盘
查看答案和解析>>
科目:高中化学 来源: 题型:
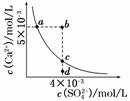 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
( )
A.在任何溶液中,c(Ca2+)、c(SO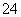 )均相等
)均相等
B.b点将有沉淀生成,平衡后溶液中c(SO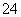 )一定等于3×10-3 mol/L
)一定等于3×10-3 mol/L
C.a点对应的Ksp等于c点对应的Ksp
D.d点溶液通过蒸发可以变到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,但存在溶解平衡。当达到平衡时,溶液中离子浓度的乘积是一个常数(此常数用Ksp表示,Ksp和水的KW相似)。如:
AgX(s) Ag++X-,Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
Ag++X-,Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
AgY(s)  Ag++Y-,Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
Ag++Y-,Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
AgZ(s)  Ag++Z-,Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
Ag++Z-,Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
下列说法错误的是( )
A.这三种物质在常温下溶解度最大的是AgZ
B.将AgY溶解于水后,向其中加入AgX,则c(Y-)减小
C.在25℃时,取0.188 g AgY(相对分子质量为188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中c(Y-)=1.0×10-4 mol/L
D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
请回答下列问题:
(1)31Ga基态原子的核外电子排布式是________________。某种半导体材料由Ga和As两种元素组成,该半导体材料的化学式是________,其晶体结构类型可能为________。
(2)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构式为
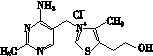
以下关于维生素B1的说法正确的是________。
A.只含σ键和π键
B.既有共价键又有离子键
C.该物质的熔点可能高于NaCl
D.该物质易溶于盐酸
(3)维生素B1晶体溶于水的过程中要克服的微粒间的作用力有________。
A.离子键、共价键
B.离子键、氢键、共价键
C.氢键、范德华力
D.离子键、氢键、范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
环保部制定的《环境空气质量标准》第二次公开征求意见结束,大家普遍赞成将PM2.5(PM2.5是指大气中直径接近于2.5×10-6 m的颗粒物)纳入常规空气质量评价,下列有关PM2.5说法不正确的是
A.PM2.5表面积大能吸附大量的有毒、有害物质
B.PM2.5在空气中形成气溶胶
C.实施绿化工程,可以有效地防治PM2.5污染
D.研制开发燃料电池汽车,降低机动车尾气污染,某种程度上可以减少PM2.5污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com