
下列叙述错误的是
A.化学反应能够制造出新的物质,但不能制造出新的元素
B.用Na2S作沉淀剂,可除去废水中的Cu2+和Hg2+
C.玻璃钢是一种合金,广泛用于汽车车身
D.只要符合限量,“食用色素”、“苯甲酸钠”、“亚硝酸盐”可以作为某些食品的添加剂
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源:2013-2014天津市第二学期期中检测高一化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是
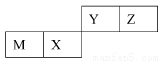
| Y | Z | |
M | X |
| |
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X 的弱
C.X 的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2 周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市南开区高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(混有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压强1.0×105 Pa、反应时间3 h):
T/K | 303 | 313 | 323 | 353 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
相应的热化学方程式如下:N2(g)+3H2O(1)==2NH3(g)+ O2(g) △H=+765.2 kJ/mol (I)
请回答下列问题:
(1)请在方框内的坐标系中,画出反应(I)在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注。
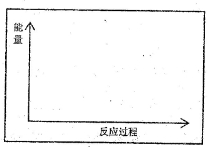
(2)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3日生成量的建议: 。
(3)写出工业上用H2和N2直接合成NH3的化学方程式 ,设在2.0 L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总物质的量之比)为4/7。计算该条件下N2的平衡转化率为 ;反应的平衡常数K= (不要求写单位)。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市南开区高三二模试卷理综化学试卷(解析版) 题型:选择题
以下有关原予结构及元素周期律的叙述正确的是
A.同主族元素从上到下,单质的熔点逐渐降低
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强
D.第IA族元素铯的两种同位素137Cs比133Cs多4个质子
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三毕业班联考二理综化学试卷(解析版) 题型:选择题
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是
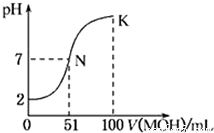
A.HA为一元强酸
B.N点水的电离程度小于K点水的电离程度
C.随着MOH溶液的滴加,比值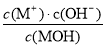 不变
不变
D.若K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市东丽区第一学期期末质量监测高一年级化学试卷(解析版) 题型:简答题
(10分)(1)向用氯化铁溶液刻制印刷电路后的废液中,加入足量铁粉,发生反应的离子方程式是 、 。
(2)实验室向某溶液中加入硫氰化钾溶液,无现象,滴加少量氯水,立即变为红色,则原溶液中含有(填离子符号) ,写出滴加氯水时发生反应的离子方程式 。
(3)我们知道,浓硫酸有脱水性、吸水性和氧化性,请写出证明浓硫酸具有氧化性的反应的化学方程式(写一个,多写若有一个错误,本题不得分) 。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市东丽区第一学期期末质量监测高一年级化学试卷(解析版) 题型:选择题
下列有关离子检验的方法正确的是
A.某溶液中加入硝酸银溶液,产生白色沉淀,该溶液中一定含有Cl-
B.某溶液中加入氢氧化钠溶液立即有白色沉淀产生,该溶液中一定有Al3+
C.某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的气体,该溶液中一定含有CO32-
D.某溶液中加入稀盐酸无现象,加入氯化钡溶液有白色溶液产生,该溶液中一定有SO42-
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高二下学期期末考试化学试卷(解析版) 题型:填空题
(14分)按要求回答下列问题:
(1)已知涤纶树脂的结构简式为: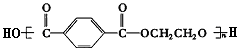
则合成涤纶树脂所需要单体的结构简式为________________和_____________
(2)已知-NH2连在苯环上显碱性,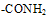 连在苯环上显中性,判断化学式为C7H7NO2的下列三种物质所具有的性质(填序号):
连在苯环上显中性,判断化学式为C7H7NO2的下列三种物质所具有的性质(填序号):
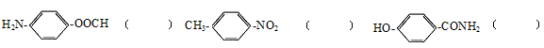
A.显中性 B.显酸性 C.显碱性
写出C7H7NO2的一种分子结构中有一个苯环,两个侧链(对位),既有酸性又有碱性物质的结构简式_____________________。
(3)下列物质中①1-丙醇 ②丙烯 ③苯酚 ④蚁酸(在下列横线上填序号)
能发生消去反应的是_________ ; 能发生加聚反应的是___________;
能发生银镜反应的是__________ ; 在空气中易被氧化变色的是__________。
(4)现有4种不同的有机物,都能燃烧生成等体积的CO2和H2O,又能都通过一步反应生成乙醇,写出对应碳原子数目要求物质的结构简式(每空只填一种)。
含2个碳原子的________________ 含3个碳原子的__________________
含4个碳原子的________________ 含6个碳原子的__________________
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高一下学期期末考试化学试卷(解析版) 题型:选择题
锗(Ge)是第四周期第 ⅣA 族元素,处于周期表中金属区与非金属区的交界线上,下列叙述正确的是
A.锗是一种金属性很强的元素
B.锗的单质具有半导体的性能
C.锗化氢(GeH4)稳定性很强
D.锗酸(H4GeO4)是难溶于水的强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com