
| A. | 100 mL 0.8 mol•L-1MgCl2溶液 | B. | 50 mL 0.5 mol•L-1AlCl3溶液 | ||
| C. | 200 mL 1 mol•L-1NaCl溶液 | D. | 200 mL 2 mol•L-1KClO3溶液 |
分析 各溶液中氯离子的物质的量浓度与溶液体积无关,氯离子浓度取决于溶质浓度及溶质化学式组成,据此进行判断.
解答 解:A.100 mL 0.8 mol•L-1MgCl2溶液中氯离子浓度为:0.8mol/L×2=1.6mol/L;
B.50 mL 0.5 mol•L-1AlCl3溶液中,氯离子的浓度为:0.5mol/L×3=1.5mol/L;
C.200 mL 1 mol•L-1NaCl溶液中,氯离子浓度为1mol/L;
D.200mL 2 mol•L-1KClO3溶液中,氯酸钾电离出钾离子和氯酸根离子,不存在氯离子;
根据分析可知,氯离子浓度最大的为A,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确离子的浓度与溶质浓度、化学式组成有关,与溶液体积无关为解答关键,D为易错点,注意氯酸钾溶液中不存在氯离子.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
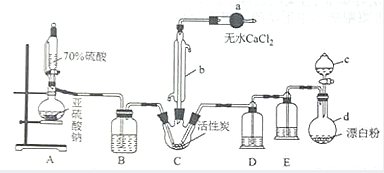 氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的实验装置如图所示:
氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 mol•L-1 HCN溶液的pH约为3 | |
| B. | HCN易溶于水 | |
| C. | 10 mL 1 mol•L-1 HCN溶液恰好与10 mL 1 mol•L-1NaOH溶液完全反应 | |
| D. | 在相同条件下,HCN溶液的导电性比强酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③⑥ | C. | ④⑤ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com