
 ,
, ×a=1-n×
×a=1-n×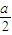 ,故a=b+c,
,故a=b+c,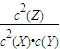 ,
,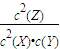 .
.

 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
| c2(Z) |
| c2(X)?c(Y) |
| c2(Z) |
| c2(X)?c(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 相关信息 |
| X | X的一种核素质量数为14,中子数为7 |
| Y | Y的过氧化物是一种淡黄色固体,可用作供氧剂 |
| Z | Z的基态原子M层电子数比L层少2个 |
| W | W的基态原子的价电子排布式为3d104sl |
查看答案和解析>>
科目:高中化学 来源:山东省青州一中2012届高三化学一轮跟踪训练:第12章第1讲原子结构(鲁科版) 题型:022
Q、W、X、Y、Z元素为前四周期元素,且原子序数依次增大,Q元素的阳离子核外无电子,W元素原子的最外层电子数是次外层电子数的2倍,Y是地壳中含量最多的元素,Z的价电子排布式为3d104s1.
(1)W位于元素周期表第________周期第________族,W的第一电离能________(填“大于”或“小于”)X的第一电离能.
(2)XQ3分子的空间构型为________,所含化学键类型为________共价键(填“极性”或“非极性”).
(3)Z的基态原子核外电子排布式是________,
Z的单质与X的最高价氧化物对应的水化物的稀溶液反应的离子方程式为________.
(4)已知:
①WQ4(g)+4XY2(g)![]() 4XY(g)+WY2(g)+2Q2Y(g) ΔH=-574 kJ·mol-1
4XY(g)+WY2(g)+2Q2Y(g) ΔH=-574 kJ·mol-1
②WQ4(g)+4XY(g)![]() 2X2(g)+WY2(g)+2Q2Y(g) ΔH=-1160 kJ·mol-1
2X2(g)+WY2(g)+2Q2Y(g) ΔH=-1160 kJ·mol-1
此温度下若用4.48 L(已折算成标准状况下)WQ4还原XY2至X2.整个过程中放出的热量为________kJ.
查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省长春市十一高中高一下学期期末考试化学试卷(带解析) 题型:填空题
(13分)已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素。
(1)W在周期表中的位置: 。
(2)在一定条件下,容积为1L密闭容器中加入1.2molX2和0.4molY2,发生如下反应:
3X2 (g) + Y2(g)  2YX3(g) △H
2YX3(g) △H
反应各物质的量浓度随时间变化如下:
①计算该温度下此反应的平衡常数K= 。
②若升高温度平衡常数K减小,则△H 0(填“>”、“<”或“=”)。
③改变下列条件,能使该平衡向正反应方向移动且平衡常数不变的是 (填字母)。
a.增大压强 b. 降低温度 c.使用催化剂 d. 增大反应物的浓度
(3)常见液态化合物X2Z2的稀溶液易被催化分解,可使用的催化剂为 (填字母)。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)A是四种元素中三种元素组成的电解质,溶液呈碱性,将常温下0.1mol·L-1的A溶液稀释至原体积的10倍后溶液的pH=12,则A的电子式为 。
(5)以X2为燃料可制成燃料电池。已知:2X2(g)+Z2(g)=2X2Z(l) △H=?572KJ·mol-1
该燃料电池释放228.8KJ电能时,生成1mol液态X2Z,该电池的能量转化率为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省德州市高三模拟检测(一模)理综化学试卷(解析版) 题型:填空题
三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是??????? 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是??????? (填物质名称);负极的电极反应式为???????????? ????????? 。
(3)C与X的单质反应生成A的化学方程式为?????????? 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= ???? 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度?????? (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g)  Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
该反应的化学平衡常数表达式是????????????? (用具体物质的化学式表示);平衡时C的转化率为???????????? 。
(6)已知:①Y2(g)+2X2(g)=2YX2(g)?  H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。
②Y2Z4(g)+X2(g)=Y2(g)+2Z2X(g)???  H=-534 kJ·mol-1。
H=-534 kJ·mol-1。
则2Y2Z4(g)+2YX2(g)=3Y2(g)+4Z2X(g)?  H=???? kJ·mol-1
H=???? kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com