
短周期元素X、Y、Z和W的原子序数依次递增,且在同一周期,四种元素原子的最外层电子数之和为19,X和Y元素原子的原子序数比6:7,X的最高正价是W的最低负价的绝对值的2倍。下列说法正确的是
A. X单质可以通过铝热法获得
B. Y的氧化物是良好的半导体材料
C. Z的氢化物比W的氢化物更稳定
D. X的氧化物和Z的最高价氧化物化合的产物中有共价键和离子键
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2016-2017学年安徽省高一上期中化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,11.2L苯中含有分子的数目为0.5NA
B.常温常压下,5.6 g乙烯(C2H4)与丁烯(C4H8)的混合物中含有的氢原子的数目为0.8NA
C.在50 g质量分数为46%的乙醇水溶液中,含有的氢原子总数为3NA
D.1mol Fe与足量的稀硫酸反应转化为Fe3+失去的电子数为3NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上期中化学试卷(解析版) 题型:选择题
雌二醇的结构简式如图,下列说法不正确的是

A.能与 Na、NaOH溶液、Na2CO3溶液反应
B.能发生加成反应、取代反应、消去反应
C.该分子中所有碳原子不可能在同一个平面内
D.可与 FeC13溶液发生显色反应,但不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省瓦房店市高三上10月月考化学试卷(解析版) 题型:推断题
X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质黄绿色有害气体。请回答下列问题:
(1)R在元素周期表中的位置为___________。
(2)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)_________________。
(3)YX4M的电子式为___________,Q3Y2与水可剧烈反应,反应的化学方程式为____________
(4)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为___________。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省瓦房店市高三上10月月考化学试卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液中c(SO42-)+c(NO3-)=2.5 mol•L-1.取200mL该混合酸,则能溶解铜的最大质量为
A.12.8g B.19.2g C.32.0g D.38.4g
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省瓦房店市高三上10月月考化学试卷(解析版) 题型:选择题
下列方程式书写正确的是
A.CaCO3的电离方程式:CaCO3=Ca2+CO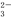
B.NaHS水解:HS-+H2O H3O++S2-
H3O++S2-
C.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
D.用少量氨水吸收工业尾气中的SO2:2NH3·H20+SO2=2NH4++SO32-+H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二上月考一化学卷(解析版) 题型:实验题
某化学探究小组为研究影 响化学反应速率的因素,进行了如下探究实验。根据实验内容完善下列实验报告。
响化学反应速率的因素,进行了如下探究实验。根据实验内容完善下列实验报告。
(1)该实验的目的为 。
(2)该实验过程中用到的玻璃仪器有 。
(3)过程体验
实验内容 | 实验现象 | 实验结论 |
(1)将两块一样大小的镁条、铁片分别同时加入等体积的0.5mol.L-1的盐酸中。 | ① 与盐酸反应产生气泡的速率快。 | 影响化学反应速率大小的内因为 ② 。 |
(2)将等体积等浓度(3mol.L-1)的盐酸两份分别同时加入盛有等质量的块状碳酸钙及粉末状碳酸钙的试管中。 | ③ 状CaCO3与盐酸反应产生气泡的速率快。 | 参加反应的固体物质颗粒 ④ ,与其他反应物的接触面积 ⑤ ,化学反应速率越快。 |
(3)分别将两块同样大小的铁片同时加入等体积不同浓度(3mol.L-1、5mol.L-1、)的盐酸中。 | 铁片与 ⑥ 盐酸反应产生气泡的速率快。 | 反应物的浓度 ⑦ ,化学反应速率越快。 |
(4)分别将两块同样大小的铁片放入盛有等体积0.5mol.L-1盐酸的甲乙两试管中,再将甲试管用酒精灯加热,对比观察现象。 | ⑧ (填“甲”或“乙”)试管中产生气泡多且快。 | 温度 ⑨ ,化学反应速率越快。 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二上月考一化学卷(解析版) 题型:选择题
25℃、101 kPa下,1g氢气燃烧生成液态水,放出142.9kJ热量,能表示H2燃烧热的热化学方程式为( )
A.2H2(g)+O2(g)==2H2O(1) △H=―571.6kJ/mol
B.2H2(g)+O2(g)==2H2O(1) △H=+571.6kJ/mol
C.H2(g)+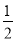 O2(g)==H2O(g) △H=―285.8kJ/mol
O2(g)==H2O(g) △H=―285.8kJ/mol
D.H2(g)+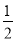 O2(g)==H2O(1) △H=―285.8kJ/mol
O2(g)==H2O(1) △H=―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二上半期考试化学卷(解析版) 题型:选择题
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
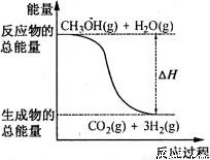
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H=-192.9kJ/mol
下列说法正确的是
A.CH3OH的燃烧热为192.9kJ·mol-1
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>—192.9kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com