
+ 4 |
A、SO
| ||
| B、Fe3+ | ||
| C、Ag+ | ||
| D、OH- |


科目:高中化学 来源: 题型:
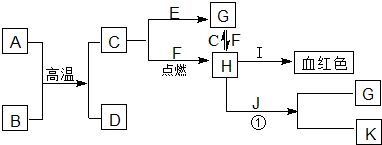
查看答案和解析>>
科目:高中化学 来源: 题型:
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关该氢氧燃料电池的说法错误的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关该氢氧燃料电池的说法错误的是( )| A、该电池工作时将化学能转化为电能 |
| B、电流从电极b经外电路流向电极a |
| C、该电池中的电极b是正极 |
| D、在电极a上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人们大量使用氟氯代烷 |
| B、人们在炼钢时向空气中排放了大量的高炉煤气 |
| C、石油炼制厂排放了大量的甲烷、氢气 |
| D、硫酸、硝酸工厂排放了大量的二氧化硫和一氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Cu+2H2SO4(浓)
| ||||
B、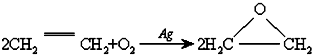 | ||||
| C、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | ||||
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用18.4mol?L-1的硫酸 |
| B、升高溶液的温度 |
| C、向溶液中加入少量铜粉 |
| D、把锌块(片)换成锌粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 步骤 | 现象 | 化学方程式 |
| 正确顺序是: |
查看答案和解析>>
科目:高中化学 来源: 题型:
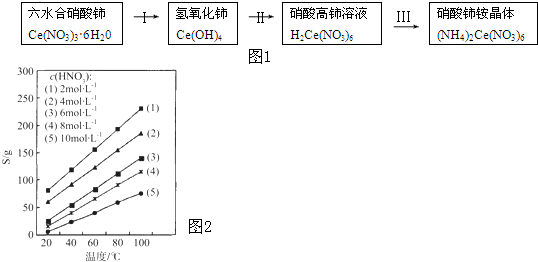
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com