
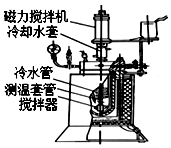
 ŹµŃéŹŅÓĆ¼ä¶žĻõ»ł±½Ķعż“߻ƼÓĒāÖʱø¼äĻõ»ł±½°·µÄŹµŃé²½ÖčČēĻĀ£ŗ
ŹµŃéŹŅÓĆ¼ä¶žĻõ»ł±½Ķعż“߻ƼÓĒāÖʱø¼äĻõ»ł±½°·µÄŹµŃé²½ÖčČēĻĀ£ŗ·ÖĪö £Ø1£©AlÓėNaOHČÜŅŗ·“Ó¦£¬æÉÓĆNaOHČÜŅŗ³żČ„£¬ÓĆĖÄĒāß»ą«Ļ“µÓµÄÄæµÄŹĒ³żČ„“߻ƼĮÖŠµÄĖ®£»
£Ø2£©“ÅĮ¦½Į°čµÄ×÷ÓĆŹĒŌö“ó·“Ó¦ĪļµÄ½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£»ĻČÓĆN2ÖĆ»»øŖÄŚæÕĘų£¬ŗóÓĆH2ÖĆ»»øŖÄŚN2£¬ŅŌĆāÖ±½ÓÓĆH2ÖĆ»»øŖÄŚæÕĘųµÄ¶ų·¢Éś±¬ÕØ£»
£Ø3£©ĪĀ¶ČøßÓŚ70”ꏱ£¬»į·¢Éśø±·“Ó¦£»
£Ø4£©½«øßŃ¹øŖĄäČ“ÖĮŹŅĪĀ£¬ŌŚH2±£»¤ĻĀ“ÓøßŃ¹øŖÖŠČ”³ö²śĘ·£®
½ā“š ½ā£ŗ£Ø1£©ŗĻ½šÖŠAlÓėNaOHČÜŅŗ·“Ó¦£ŗ2Al+2NaOH+2H2O=2NaAlO2+3H2”ü£»ÓĆĖÄĒāß»ą«Ļ“µÓµÄÄæµÄŹĒ³żČ„“߻ƼĮÖŠµÄĖ®£®¹Ź“š°øĪŖ£ŗAl£» ³żČ„“߻ƼĮÖŠµÄĖ®£»
£Ø2£©“ÅĮ¦½Į°čµÄ×÷ÓĆŹĒŌö“ó·“Ó¦ĪļµÄ½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£»ĻČÓĆN2ÖĆ»»øŖÄŚæÕĘų£¬ŗóÓĆH2ÖĆ»»øŖÄŚN2£¬ŅŌĆāÖ±½ÓÓĆH2ÖĆ»»øŖÄŚæÕĘųµÄ¶ų·¢Éś±¬ÕØ£»¹Ź“š°øĪŖ£ŗŌö“ó·“Ó¦ĪļµÄ½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£»·ĄÖ¹Ö±½ÓĶØČėH2Ź±·¢Éś±¬ÕØ£»
£Ø3£©ĪĀ¶ČøßÓŚ70”ꏱ£¬ŌĮĻµÄĄūÓĆĀŹæŖŹ¼½µµĶĘäÖ÷ŅŖŌŅņŹĒ»į·¢Éśø±·“Ó¦£¬ČēH2ŗĶ±ūĶŖ·¢Éś¼Ó³É·“Ó¦£¬¹Ź“š°øĪŖ£ŗĪĀ¶ČøßÓŚ70”ꏱH2ŗĶ±ūĶŖ·¢Éś¼Ó³É·“Ó¦£»
£Ø4£©²½Öč3ÖŠ½ųŠŠŹŹµ±µÄ²Ł×÷ĪŖ½«øßŃ¹øŖĄäČ“ÖĮŹŅĪĀ£¬ŌŚH2±£»¤ĻĀ“ÓøßŃ¹øŖÖŠČ”³ö²śĘ·£¬·Åµō²ŠÓąĘųĢ壬¹Ź“š°øĪŖ£ŗ½«øßŃ¹øŖĄäČ“ÖĮŹŅĪĀ£¬·Åµō²ŠÓąĘųĢ壮
µćĘĄ ±¾Ģāæ¼²éĮĖ¼äĻõ»ł±½°·ÖʱøµÄŹµŃé·½°øÉč¼Ę”¢ŹµŃé×°ÖƵĥķ½āĘĄ¼Ū”¢ÉųĪöŌĄķµÄÓ¦ÓĆµČ£¬ŹĒ¶ŌĖłŃ§ÖŖŹ¶µÄ×ŪŗĻŌĖÓĆ£¬×¢Ņā»ł“”ÖŖŹ¶µÄÕĘĪÕ£¬±¾ĢāÄѶČÖŠµČ£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃéÄæµÄ | ŹµŃé²Ł×÷ |
| A | ÅäÖĘCuSO4ČÜŅŗ | ½«ĮņĖįĶ¾§ĢåČÜÓŚČČĖ®ÖŠ£¬Č»ŗóĻ”ŹĶ |
| B | ³żČ„ŹŌ¹ÜÄŚ±ŚµÄŅų¾µ | ¼ÓČėÅØ°±Ė®½žÅŻ£¬ŌŁÓĆÕōĮóĖ®Ļ“µÓ |
| C | Ģį“æŗ¬ÉŁĮæŅŅĖįµÄŅŅ“¼£ØŅŅ“¼·Šµć78.5”ę£© | ¼ÓČėÉśŹÆ»Ņŗó½ųŠŠÕōĮó£¬ŹÕ¼Æ78.5”ęĮó·Ö |
| D | ””Ö¤Ć÷HClOĪŖČõĖį | ÓĆ½ą¾»µÄ²£Į§°ōÕŗČ”NaClOČÜŅŗŌŚpHŹŌÖ½ÉĻ£¬“żŹŌÖ½±äÉ«ŗóÓė±ź×¼±ČÉ«¶ŌÕÕ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę½ŗāŹ±£¬X µÄ×Ŗ»ÆĀŹĪŖ50% | |
| B£® | øĆĪÕ¶ČĻĀĘ½ŗā³£ŹżK=10£Ø10mol•L-1£©-1 | |
| C£® | 10minÄŚÉś³ÉĪļZ µÄ·“Ó¦ĖŁĀŹ0.02mol•L-1•min-1 | |
| D£® | ČōYŹĒÓŠÉ«ĘųĢå£¬Ö»Ń¹ĖõČŻĘ÷µÄĢå»ż£¬ŌņĢåĻµŃÕÉ«±äĒ³ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀøÉŌļµÄCl2ÄÜÓĆøÖĘæÖüŌĖ | |
| B£® | ¼ģŃéHClĘųĢåÖŠŹĒ·ń»ģÓŠCl2£¬·½·ØŹĒ½«ĘųĢåĶØČėĻõĖįŅųČÜŅŗ | |
| C£® | SiO2æÉÓĆÓŚÖʱø¹āµ¼ĻĖĪ¬ | |
| D£® | HFČÜŅŗ²»ÄÜÖü“ęŌŚÄ„æŚ²£Į§ČūµÄŹŌ¼ĮĘæÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪžÉüŃō¼«µÄŅõ¼«±£»¤·ØŹĒÓ¦ÓƵē½āŌĄķ·ĄÖ¹½šŹōµÄøÆŹ“ | |
| B£® | AlCl3ČÜŅŗŗĶAl2£ØSO4£©3ČÜŅŗ·Ö±š¼ÓČČÕō·¢£¬ĖłµĆ¹ĢĢåµÄ³É·ÖĻąĶ¬ | |
| C£® | ŹŅĪĀŹ±½«Na2CO3ČÜŅŗ¼ÓĖ®Ļ”ŹĶŗó£¬ŌŁ»Öø“ÖĮŹŅĪĀ£¬pHŗĶKW¾ł¼õŠ” | |
| D£® | CO£Øg£©µÄČ¼ÉÕČČŹĒ283.0kJ/mol£¬Ōņ2CO2£Øg£©=2CO£Øg£©+O2£Øg£©·“Ó¦µÄ”÷H=+2”Į283.0kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅØŃĪĖį | B£® | ÅØĻõĖį | C£® | ÅØĮņĖį | D£® | ĒāŃõ»ÆÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

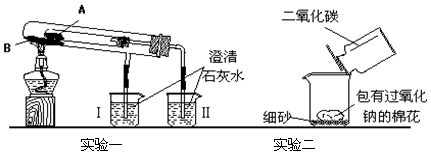
| A£® | Ō×Ó°ė¾¶£ŗZ£¾Y£¾X | |
| B£® | RŌŖĖŲµÄŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļŗĶWŌŖĖŲµÄŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ£¬ĖįŠŌĒ°ÕßĒæ | |
| C£® | XŗĶZŠĪ³ÉµÄ»ÆŗĻĪļÄÜČÜÓŚNaOHČÜŅŗ | |
| D£® | YŗĶXŠĪ³ÉµÄ»ÆŗĻĪļÖŠ£¬ŅõŃōĄė×ÓµÄøöŹż±ČæÉÄÜĪŖ1£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
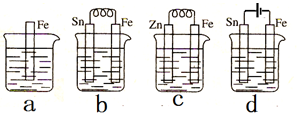
| A£® | ×°ÖĆbÖŠSn¼«ø½½üČÜŅŗµÄpH½«¼õŠ” | |
| B£® | ×°ÖĆcÖŠÓĆŠæ±£»¤ĢśµÄ·½·Ø³ĘĪŖĪžÉüŅõ¼«µÄŃō¼«±£»¤·Ø | |
| C£® | ×°ÖĆdÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖFe+2H+$\frac{\underline{\;µē½ā\;}}{\;}$Fe2++H2”ü | |
| D£® | Ķ¼a”¢b”¢c”¢dÖŠ“æĢś±»øÆŹ“µÄĖŁĀŹÓÉæģµ½ĀżµÄĖ³ŠņŹĒb£¾a£¾c£¾d |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com