
有机物A的分子中碳氢原子数之比为1:2。它不与碳酸钠反应,相同物质的量的A与氢气的质量比为37:1,0.37g A与足量的银氨溶液反应可析出1.08g Ag.A在一定条件下与氢气反应生成B,1mol B 与足量金属钠反应可产生22.4LH2(标准状况下),B不与碳酸钠反应.试写出A、B可能的结构简式。
科目:高中化学 来源:2016-2017学年云南省高一上期中化学试卷(解析版) 题型:选择题
下列有关0.1mol/LKNO3溶液的叙述正确的是( )
A.在1L水中溶解10.1g KNO3,即可配制得0.1mol/L KNO3溶液
B.100mL该溶液中含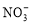 0.1mol
0.1mol
C.从1L该溶液中取出100mL,所取出的KNO3溶液的浓度为0.01mol/L
D.1L该溶液中含KNO3101g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:选择题
按碳骨架分类,下列说法正确的是
A.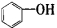 属于醇类化合物 B.
属于醇类化合物 B.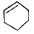 属于芳香族化合物
属于芳香族化合物
C.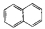 属于脂环化合物 D.CH3CH(CH3)2属于链状化合物
属于脂环化合物 D.CH3CH(CH3)2属于链状化合物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
水的电离平衡曲线如下图所示,下列说法不正确的是
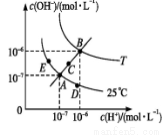
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
某温度下,向2L恒容密闭容器中充入1.0molA和1.0molB,发生反应A(g)+B(g) C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是

A.反应在前5s的平均速率v(A)= 0. 17mol/(L·s)
B.保持其他条件不变,升高温度,平衡时c(A)=0.41mol/L,则反应的△H>0
C.相同温度下,起始时向容器中充入2.0molC,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 molA、0.20 molB和1.0 molC,反应达到平衡前v(正)<v(逆)
molC,反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:推断题
有7瓶有机物A、B、C、D、E、F、G,它们可能是苯、甲苯、己烯、苯酚、乙醇、乙醛、乙酸,为确定每瓶成分,进行下列实验:
①取7种少量有机物,分别加水,振荡后与水分层的是A、D、G;
②取少量A、D、G分别加入溴水,振荡后,只有D能使溴水褪色,且有机层为无色;
③取少量A、G,分别加入酸性KMnO4溶液,振荡后,G能使酸性KMnO4溶液褪色;
④取A少量加入浓H2SO4和浓HNO3,加热后倒入水中,有苦杏仁味黄色油状液体生成;
⑤取少量B、C、E、F,分别加入银氨溶液,经水浴加热后,只有B出现银镜;
⑥取少量C、E、F,若分别加入金属钠,均有H2放出;若分别加入Na2CO3溶液,只有F有气体放出;
⑦取少量C、E,滴入浓溴水,E生成白色沉淀;
⑧取少量C、F,混合后加入浓H2SO4,加热后有果香味的油状液体生成.
(1) 试推断A﹣G各是什么物质?写出它们的分子式。
A , C , F ,G .
(2)写出实验⑤反应的化学方程式 .
(3)写出实验⑦反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:选择题
某种橡胶分解产物为碳氢化合物,对这种碳氢化合物作如下实验:
① 若取一定量完全燃烧,使燃烧后的气体通过干燥管,干燥管增重0.72 g,再通过石灰水,石灰水增重2.2 g。
② 经测定,该碳氢化合物( 气体)的密度是相同条件下氢气密度的34倍。
气体)的密度是相同条件下氢气密度的34倍。
③ 该碳氢化合物0.1 mol能和32 g溴起加成反应.
④ 经分析,在③的生成物中,溴原子分布在不同的碳原子上,且溴代物中有一个碳原子在支链上。下列说法正确的是( )
A.该碳氢化合物为2-甲基-1,3-戊二烯
B.该碳氢化合物与溴单质1:1加成时可以生成3种不同的产物
C.该碳氢化合物与溴单质1:1加成时可以生成2种不同的产物
D.该碳氢化合物与足量氢气加成时可以生成正戊烷
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上期中化学卷(解析版) 题型:实验题
某学生用0.1mol/L  KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞;
(B)用标准溶液润洗滴定管2-3次;
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm;
(E)调节液面至0或0刻度以下,记下读数;
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度;
完成以下填空:
(1)正确操作的顺序是:(用序号字母填写)B、D、_______________.
(2)上述(B)操作的目的是_____________________。
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)_________________。
(4)实验中用左手控制 (填仪器及部位),眼睛注视 ,直至滴定终点。判断到达终点的现象是 。
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:选择题
按如图所示的装置进行电解实验。A极是铜镍合金,B极为纯铜,电解质溶液为硫酸铜溶液(足量)。通电一段时间后,A极恰好全部溶解,此时B极质量增加3.2g,溶液质量增加0.05 g,(已知氧化性,Cu2+>Ni2+)则A合金中铜、镍原子个数比为
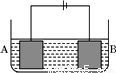
A.4∶1 B.3∶1 C.2∶1 D.1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com