
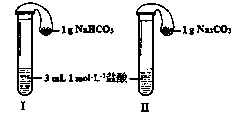
| ʵ�鷽�� | Ԥ������ | Ԥ������ |
| ����1����2 mL Na2CO3��Һ�еμ�1 mL 0��5 mol��L-1CaCl2��Һ | �а�ɫ���� | Na2CO3��Һ�е�CO32-Ũ�Ƚϴ�����CaCl2������ӦCa2+ + CO32- = CaCO3���� |
| ����2����2 mL NaHCO3��Һ�еμ�1 mL 0��5 mol��L-1CaCl2��Һ | �ް�ɫ���� | NaHCO3��Һ�е�CO32-Ũ�Ⱥ�С��������CaCl2��Ӧ�� |
 Na2CO3+ CO2��+H2O��
Na2CO3+ CO2��+H2O�� Na2CO3+ CO2��+H2O�� (2) �ٸ���ʵ������õ��Ľ����ǣ�����ͬ���¶��£�Na2CO3��NaHCO3�����ܽ���ˮ�С���ʢ��Na2CO3���ձ��г��ֵ�������b����Һ�¶����� ��d�������̪��ʺ�ɫ������ѡ��Ϊ��b d�� (3) Na2CO3�����ᷴӦ�ֲ����С�������HCl+Na2CO3=NaHCO3 +NaCl�����������塣Ȼ����HCl+ NaHCO3 =" NaCl+" CO2��+H2O�����Ԣ�Ȣ�Ӧ�ķų�����Ҫ�졣����̶ȸ�Ϊ���ҡ��� ���ݼ����֪��NaHCO3 +HCl= CO2��+H2O +NaCl �������尴��NaHCO3���㡣��2HCl+Na2CO3= CO2��+H2O +2NaCl���ų����巴Ӧ�ų����尴��HCl�����㡣��������ͬʱNaHCO3��Ӧ����������ࡣ����ѡ��Ϊ��a��(4) ����2����2 mL NaHCO3��Һ�еμ�1 mL 0��5 mol��L-1CaCl2��Һ,������ɫ���������塣����ΪHCO3-����Һ�мȴ��ڵ��� Ҳ������ˮ��ƽ�⣬���������̼�������������ӽ���γ�̼��Ƴ�����ˮ�������̼��ﵽһ�����ͷ����ֽⷴӦ����������̼��ˮ����������£�NaHCO3��Һ��CaCl2��Һ��Ӧ�����ӷ���ʽΪ: Ca2++2HCO3-= CaCO3��+ CO2��+H2O��2CO3��NaHCO3�����ʵ�֪ʶ��
Na2CO3+ CO2��+H2O�� (2) �ٸ���ʵ������õ��Ľ����ǣ�����ͬ���¶��£�Na2CO3��NaHCO3�����ܽ���ˮ�С���ʢ��Na2CO3���ձ��г��ֵ�������b����Һ�¶����� ��d�������̪��ʺ�ɫ������ѡ��Ϊ��b d�� (3) Na2CO3�����ᷴӦ�ֲ����С�������HCl+Na2CO3=NaHCO3 +NaCl�����������塣Ȼ����HCl+ NaHCO3 =" NaCl+" CO2��+H2O�����Ԣ�Ȣ�Ӧ�ķų�����Ҫ�졣����̶ȸ�Ϊ���ҡ��� ���ݼ����֪��NaHCO3 +HCl= CO2��+H2O +NaCl �������尴��NaHCO3���㡣��2HCl+Na2CO3= CO2��+H2O +2NaCl���ų����巴Ӧ�ų����尴��HCl�����㡣��������ͬʱNaHCO3��Ӧ����������ࡣ����ѡ��Ϊ��a��(4) ����2����2 mL NaHCO3��Һ�еμ�1 mL 0��5 mol��L-1CaCl2��Һ,������ɫ���������塣����ΪHCO3-����Һ�мȴ��ڵ��� Ҳ������ˮ��ƽ�⣬���������̼�������������ӽ���γ�̼��Ƴ�����ˮ�������̼��ﵽһ�����ͷ����ֽⷴӦ����������̼��ˮ����������£�NaHCO3��Һ��CaCl2��Һ��Ӧ�����ӷ���ʽΪ: Ca2++2HCO3-= CaCO3��+ CO2��+H2O��2CO3��NaHCO3�����ʵ�֪ʶ��

 С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʱ������ų� |
| B���μ�����ʱ������������ |
| C������ˮ��μ��Ȼ�����Һ���а�ɫ�������� |
| D������ˮ��μӳ���ʯ��ˮ���а�ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ֱ���������İ�ɫ��ĩ�мӵ����������ˮ���ȽϹ����ܽ����Ķ��� |
| B���ֱ������Һ������Ca(OH)2��Һ���Ƚ��Ƿ��г������� |
| C���ֱ������Һ������ɫ��Ӧ���۲�������ɫ |
| D���ֱ����İ�ɫ��ĩ������ͼװ�ý���ʵ�飬�Ƚϳ���ʯ��ˮ�Ƿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ӧ������ú���У�ʵ���ʣ�������Ż�ԭƿ |
| B��2��3g����97��7g ˮ��Ӧ����Һ�����ʵ�������������4% |
| C������CuSO4��Һ��Ӧ���ɵ���ɫ��������ʱ���ְ��ߣ����������Ľ���ͭ |
| D����һ��Ļ�ѧ��ԭ��������ȡ�����ƣ������õ���ۻ�NaCl�ķ����Ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ƹ���ˮ�棬�ۻ�����ɫ������С�� | B����������ú���� |
| C��������Һ����������Ϊ2.25�� | D����Ӧ��ת��0.1mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ȡa�˻�����ּ��ȣ�����b�� |
| B��ȡa�˻����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b�˹��� |
| C��ȡa�˻����������ϡ�����ַ�Ӧ���ݳ������ü�ʯ�����գ�����b�� |
| D��ȡa�˻����������Ba(OH)2��Һ��ַ�Ӧ�����ˡ�ϴ�ӡ���ɣ���b�˹��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
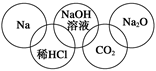
| A���ֽⷴӦ | B�����ֽⷴӦ |
| C�����Ϸ�Ӧ | D���û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
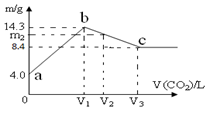
| A���������ʣ�a����NaOH��b����Na2CO3��c����NaHCO3 |
| B��a��b �� b��c ���ι��̵õ��ľ��壬������ͬ�ľ������� |
| C�����������е���Һ��һ�����ں��ʽ��c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-) |
| D����ͨ��V2=1��344 L (���) ���壬��m2=13��12 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Al��ʣ�� | B��c(Na+)=c(AlO-2) |
| C����������Ϊ2 mol | D��c(Na+)=c(Al3+) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com