
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:阅读理解
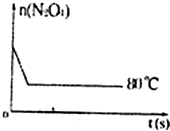
| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |


查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第16期 总第172期 人教课标版 题型:013
|
向某溶液中通入 NO2,一段时间后,在该溶液中一定能大量共存的离子组是 | |
| [ ] | |
A. |
Na+、H+、SO42-、I- |
B. |
Na+、Ca2+、CO32-、Al3+ |
C. |
Na+、K+、Fe2+、H+ |
D. |
K+、SO42-、Cl-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
为改善大气质量,国家拟于“十二五”期间,力争将CO2变为燃料或有机化学产品的构想变为现实,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。
I.目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。写出甲烷直接将NO2还原得到无污染的产物的化学方程式 。
(2)降低汽车尾气的方法之一是在排气管上安装催化
转化器,发生如下反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。
该反应的化学平衡常数表达式为K= 。
在一定温度下,将2molNO、1molCO充入1L
 固定容积的容器中,反应过程中各物质的浓度变化
固定容积的容器中,反应过程中各物质的浓度变化
如下图所示。
若保持温度不变,20min时再向容器中充入
CO、N2各0.6mol,平衡将 移动(填“向左”、 “向右”或“不”)。
若20min时改变反应条件,导致N2浓度发生如右图所示的变化,则改变的条件可能
是 (填序号)。
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
 (3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如右图,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,写出负极反应式为 。用这种方法处理SO2废气的优点是可回收大量有效能,副产品为H2SO4,减少环境污染。
(3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如右图,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,写出负极反应式为 。用这种方法处理SO2废气的优点是可回收大量有效能,副产品为H2SO4,减少环境污染。
II.有人提出用碳酸钠溶液吸收发电厂废气中的二氧化硫。
已知:H2SO3的电离平衡常数为 K1=1.54×10-2 ,K2=1.O2×10-7
H2CO3的电离平衡常数为K1=4.31×l0-7 K2=5.61×10-11
(4)请写出向碳酸钠溶液中通入一定量的SO2生成无污染的二氧化碳气体的的化学方程式
查看答案和解析>>
科目:高中化学 来源:2009-2010学年山东省临沂市高三(上)期末化学试卷(解析版) 题型:解答题
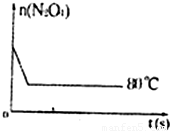
| 时间(s) n(mol) | 20 | 40 | 60 | 80 | 100 | |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com