
(1)[2013·新课标全国卷Ⅰ,28(3)]二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:(ⅰ)CO(g)+2H2(g)===CH3OH(g)
ΔH1=-90.1 kJ·mol-1
(ⅱ)CO2(g)+3H2(g)===CH3OH(g)+H2O(g)
ΔH2=-49.0 kJ·mol-1
水煤气变换反应:(ⅲ)CO(g)+H2O(g)===CO2(g)+H2(g)
ΔH3=-41.1 kJ·mol-1
二甲醚合成反应:(ⅳ)2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ·mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为________________。
(2)[2013·四川理综,11(5)节选]焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)??2SO3(g)
ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)
ΔH3=-545 kJ·mol-1。
则SO3(g)与H2O(l)反应的热化学方程式是________。
(3)[2013·浙江理综,27(1)]捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)??(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)??NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)??2NH4HCO3(aq)ΔH3
ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=________。
(4)[2013·天津理综,10(2)①]为减少SO2的排放,常采取的措施有:
将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1
C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:__________________________________________。
(5)[2013·北京理综,26(2)①]汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
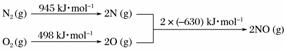
写出该反应的热化学方程式:______________________________________________________。
答案 (1)2CO(g)+4H2(g)===CH3OCH3(g)+H2O(g) ΔH=-204.7 kJ·mol-1
(2)SO3(g)+H2O(l)===H2SO4(l)
ΔH=-130 kJ·mol-1
(3)2ΔH2-ΔH1
(4)C(s)+H2O(g)===CO(g)+H2(g)
ΔH=+131.3 kJ·mol-1
(5)N2(g)+O2(g)===2NO(g) ΔH=+183 kJ·mol-1
解析 (1)筛选用热化学方程式为(ⅰ)和(ⅳ),
用(ⅰ)×2+(ⅳ)即可得目标方程式:
2CO(g)+4H2(g)===CH3OCH3(g)+H2O(g)
ΔH=-204.7 kJ·mol-1。
(2)根据盖斯定律,得出SO3(g)+H2O(l)===H2SO4(l) ΔH4只须按下式进行即可:
ΔH= (ΔH3-ΔH1-2ΔH2)=-130 kJ·mol-1,
(ΔH3-ΔH1-2ΔH2)=-130 kJ·mol-1,
热化学方程式应为
SO3(g)+H2O(l)===H2SO4(l) ΔH=-130 kJ·mol-1。
(3)Ⅱ式×2-Ⅰ式,即可得反应Ⅲ。
(4)下式减上式即可求得热化学方程式。
(5)拆开化学键吸收能量,形成化学键释放能量
N2(g)+O2(g)===2NO(g)其ΔH计算方法如下:
ΔH=945 kJ·mol-1+498 kJ·mol-1-2×630 kJ·mol-1=+183 kJ·mol-1。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是( )
A.CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=+890.3 kJ·mol-1
B.CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.3 kJ·mol-1
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.3 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。
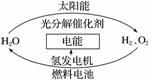
下列说法正确的是( )
A.H2O的分解反应是吸热反应
B.氢能源已被普遍使用
C.2 mol 液态H2O具有的总能量低于2 mol H2和1 mol O2的能量
D.氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:P4(g)+6Cl2(g)===4PCl3(g),
ΔH=a kJ·mol-1,
P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1,
P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ·mol-1,PCl3中P—Cl键的键能为1.2c kJ·mol-1。
下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能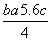 kJ·mol-1
kJ·mol-1
D.P—P键的键能为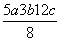 kJ·mol-1
kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
①H2(g)+ O2(g)===H2O(g) ΔH1=a kJ·mol-1
O2(g)===H2O(g) ΔH1=a kJ·mol-1
②2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1
③H2(g)+ O2(g)===H2O(l) ΔH3=c kJ·mol-1
O2(g)===H2O(l) ΔH3=c kJ·mol-1
④2H2(g)+O2(g)===2H2O(l) ΔH3=d kJ·mol-1
下列关系式中正确的是( )
A.a<c<0 B.b>d>0
C.2a=b<0 D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)2013年以来,全国很多地区都曾陷入严重的雾霾和污染天气中,冬季取暖排放的CO2、汽车尾气等都是形成雾霾的因素。
已知:①N2(g)+O2(g)===2NO(g)
ΔH=+179.5 kJ·mol-1
②2NO(g)+O2(g)===2NO2(g)
ΔH=-112.3 kJ·mol-1
③2NO(g)+2CO(g)===N2(g)+2CO2(g)
ΔH=-759.8 kJ·mol-1
下图是在101 kPa,298 K条件下1 mol NO2和1 mol CO反应生成1 mol CO2和1 mol NO过程中能量变化的示意图。则a=________。

(2)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:CO2+H2O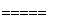 CO+H2+O2
CO+H2+O2
已知:


①反应Ⅱ是______反应(填“吸热”或“放热”),其原因是
________________________________________________________________________。
②反应A的热化学方程式是____________。
(3)一定条件下,在容积为3 L的密闭容器中反应:CO(g)+2H2(g)??CH3OH(g)达到化学平衡状态。
根据题目有关信息,请在右下坐标图中标示出该化学反应过程的能量变化(标明信息)。
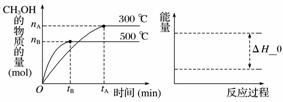
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D都是短周期元素。A的原子核外有两个电子层,最外层已达到饱和。B位于A元素的下一周期,最外层的电子数是A最外层电子数的1/2。C的离子带有两个单位正电荷,它的核外电子排布与A元素原子相同。D与C属同一周期,D原子的最外层电子数比A的最外层电子数少1。
(1)根据上述事实判断:A是________,B是________,C是________,D是________。
(2)C的离子的核外电子排布式为________________;D原子的核外电子排布式为______________。
(3)B位于第________周期________族,它的最高价氧化物的化学式是__________,最高价氧化物的水化物是一种________酸。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com